��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ڻ�ѧ��Ӧ�У������Ӧǰ��Ԫ�صĻ��ϼ۷����仯����һ����______ת�ƣ����෴Ӧ������______��Ӧ��Ԫ�ػ��ϼ����ߣ�������Ԫ�ص�ԭ��______���ӣ�����Ԫ�ص����ʷ���______��Ӧ������������______����������Fe3O4+4CO
3Fe+4CO2���У�����������______�ǻ�ԭ����
�ο��𰸣�������ԭ��Ӧ����������Ԫ�صĻ��ϼ۷����仯��ʵ���ǵ���ת�ƣ��л��ϼ۱仯�ķ�Ӧ��������ԭ��Ӧ�����ϼ�����Ԫ��ʧ���ӣ�������������������Ӧ�����и�Ԫ�صķ�Ӧ���ǻ�ԭ�������ϼ۽���Ԫ�صõ����ӣ�����ԭ������ԭ��Ӧ�����и�Ԫ�صķ�Ӧ�������������ʴ�Ϊ�����ӣ�������ԭ��ʧ����������ԭ��Fe3O4��CO��
���������
�����Ѷȣ�һ��
2��ѡ���� Ԫ��R�����·�Ӧ��RO3-+5R-+6H+�T3R2+3H2O������˵����ȷ���ǣ�������
A��Ԫ��Rλ�����ڱ��еڢ�A��
B��RO3-�е�Rֻ�ܱ���ԭ
C��R2�ڳ��³�ѹ��һ��������
D��ÿ��Ӧ����1molRO3-��ת�Ƶ��ӵ����ʵ���Ϊ5mol
�ο��𰸣�A������RԪ�ص�һ������R-����֪��Ԫ�ص����Ϊ+7�ۣ�Ԫ��Rλ�����ڱ��еڢ���A�壬��A����
B��RO3-��RԪ�صĻ��ϼ�Ϊ+5�ۣ������+7�ۣ�����RO3-�е�R���ܱ���ԭ���ܱ���������B����
C�����ڱ��еڢ���A����嵥����Һ̬����C����
D����ӦRO3-+5R-+6H+�T3R2+3H2O�У�RԪ�صĻ��ϼ�Ϊ+5�ۣ���Ϊ0�ۣ����ϼ۽���5������ת�Ƶ�����Ϊ5����ÿ��Ӧ����1molRO3-��ת�Ƶ��ӵ����ʵ���Ϊ5mol����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3������� д�����з�Ӧ��˫���ţ���ָ���������ͻ�ԭ�����Լ���ʧ�ĵ�������
��1��2KClO3
2KCl+O2��
��2��4P+5O22P2O5��
�ο��𰸣���1����Ӧ��ClԪ�ػ��ϼ���+5�۽���ΪKCl��-1�ۣ���Ԫ����-2������ΪO2��0�ۣ��������ͻ�ԭ������KClO3��ת�Ƶ�����Ϊ12����˫���ű�ʾ�����ת�����Ϊ��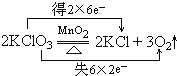 ��
��
�ʴ�Ϊ�� ��
��
��2����Ӧ��PԪ�ػ��ϼ���0�����ߵ�+5�ۣ�OԪ�ػ��ϼ���0�۽��͵�-2�ۣ�������ΪO2����ԭ��ΪP����˫���ű�ʾ�����ת�����Ϊ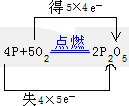 ��
��
�ʴ�Ϊ�� ��
��
���������
�����Ѷȣ���
4������� ʵ���ҿ���KMnO4��Ũ���ᷴӦ��ȡ��������仯�ɱ���Ϊ��
______KMnO4+______HCl��Ũ���T______KCl+______MnCl2+______Cl2��+____________
��1������ɸû�ѧ����ʽ����ƽ��δ֪�ﻯѧʽ�ͻ�ѧ������������ڣ���
��2���뽫������ƽ�Ļ�ѧ����ʽ��дΪ���ӷ���ʽ______��
��3��Ũ�����ڷ�Ӧ����ʾ������������______����д��ţ���ѡ���ۣ���
��ֻ�л�ԭ��?�ڻ�ԭ�Ժ�����
��ֻ��������?�������Ժ�����
��4������0.1molCl2����ת�Ƶĵ��ӵ����ʵ���Ϊ______mol��
��5��ClO2���к�ǿ�������ԣ���ˣ�������������������������Ч�ʣ��Ե�λ�����õ��ĵ���������������Cl2��______����
�ο��𰸣���1��Ԫ�ػ��ϼ۵ı仯�ֱ�Ϊ��MnԪ����KMnO4��+7�۱��MnCl2�е�+4�ۣ����ϼ۽��ͣ�����KMnO4����������һ��KMnO4��5����������MnCl2��
ClԪ����?HCl�е�-1�۱��Cl2�е�0�ۣ����ϼ����ߣ�����?HCl�ǻ�ԭ��������һ��Cl2������ʧ2�����ӣ�
����������ԭ��Ӧ�е�ʧ��������ȣ�����С��������10�����Եõ�10mol������Ҫ5mol������زμӷ�Ӧ��ʧȥ1omol������Ҫ10molHCl�μ�������ԭ��Ӧ���ٸ���ԭ���غ㣬�ж��������ʵļ�������
�ʴ�Ϊ��2��10�� 2��2��5��8
?��2�����ʡ��������д��ѧʽ��ǿ�����д���ӣ��ʴ�Ϊ��2MnO4-+16H++10Cl-�TMn2++5Cl2��+8H2O
��3��ͨ�����Ϸ���֪��������ԭ�������ã�������ǿ�ᣬ�ܺͽ��������ﷴӦ�����κ�ˮ��������������ã�
��ѡ����
��4��2MnO4-+16H++10Cl-�TMn2++5Cl2��+8H2O?ת�Ƶ���
? 5mol? 10mol
?0.1mol? 0.2mol
�ʴ�Ϊ��0.2mol
��5��Cl2��ClO2��������ʱ���仹ԭ�����ΪCl-�����ݵõ��������ã�
5NA67.5��2NA71=2.63
�ʴ�Ϊ��2.63
���������
�����Ѷȣ�һ��
5��ѡ���� ��ֻ֪��Ũ������MnO2�ڼ��ȵ������²��ܷ�Ӧ����C12��ϡ������MnO2����Ӧ�������ڿ���������ʾʵ��ʱ�����������ַ�����ȡC12�����ú�HCl?146g��Ũ������174g?MnO2��Ӧ������87g?MnO2��������Ũ���ᷴӦ��������C12��������
A���ٱȢڶ�
B���ڱȢٶ�
C��һ����
D�����Ƚ�
�ο��𰸣���Ӧ�Ļ�ѧ����ʽΪ��4HCl��Ũ��+MnO2?��?.?MnCl2+Cl2��+H2O��
��n��HCl��=146g36.5g/mol=4mol��n��MnO2��=174g87g/mol=2mol��
Ũ������MnO2������ѧ��Ӧ�����ŷ�Ӧ�Ľ��У������Ũ�Ƚ��ͣ���ԭ�Լ�����ϡ������MnO2����Ӧ���������ɵ�n��Cl2����1mol��
��n��MnO2��=87g87g/mol=1mol������Ũ�������������ɵ�n��Cl2��=1mol��
��������C12�ڱȢٶ࣬
��ѡB��
���������
�����Ѷȣ�һ��