��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б����У����������ǣ�������
A���е���ת�ƣ���ʧ��ƫ�ƣ��Ļ�ѧ��Ӧ����������ԭ��Ӧ
B�������ǽ�����ת��Ϊ��ѧ�ܵ�װ��
C������������������ɢϵ�ĸ���ԭ���ǽ�����ж����ЧӦ
D��Ԫ�ص���������Ԫ��ԭ�������ĵ��������������Ա仯
�ο��𰸣�A��������ԭ��Ӧ��ʵ���ǵ��ӵ�ת�ƣ��е���ת�ƣ���ʧ��ƫ�ƣ��Ļ�ѧ��Ӧ����������ԭ��Ӧ����A��ȷ��
B�������ǽ�����ת��Ϊ��ѧ�ܵ�װ�ã���B��ȷ��
C������������������ɢϵ�ĸ���ԭ���Ƿ�ɢ�����Ĵ�С����C����
D��Ԫ�������ɣ�Ԫ�ص���������Ԫ��ԭ�������ĵ��������������Ա仯�����ʣ���D��ȷ��
��ѡC��
���������
�����Ѷȣ���
2������� �������з�Ӧ��5KCl+KClO3+3H2SO4=3Cl2��+3K2SO4+3H2O���ݴ�����
��1������÷�Ӧ�е��ӵ�ת�Ʒ������Ŀ��5KCl+KClO3+3H2SO4=3Cl2��+3K2SO4+3H2O
��2���÷�Ӧ����������______��
��3���÷�Ӧ�����������뻹ԭ�������������______��
��4������Ӧ����0.3mol?Cl2ʱ����ת�Ƶĵ��ӵ����ʵ�����______��
�ο��𰸣���1���÷�Ӧ���Ȼ�������Ԫ�ػ��ϼ���-1�۱�Ϊ0�ۣ����������Ԫ�صĻ��ϼ���+5�۱�Ϊ0�ۣ�������ת�Ƶ�������5��
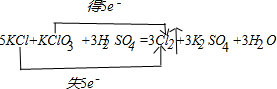
��
�ʴ�Ϊ��
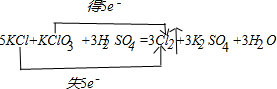
��
��2���÷�Ӧ�У����������Ԫ�صĻ��ϼ���+5�۱�Ϊ0�ۣ���������������������ʴ�Ϊ��KClO3��
?��3���÷�Ӧ�л�ԭ�����Ȼ��أ�������������أ���������������������ԭ����Ҳ����������������ͻ�ԭ���������֮����5��1���ʴ�Ϊ��5��1��
��4������Ӧ����0.3mol?Cl2ʱ����ת�Ƶĵ��ӵ����ʵ���=0.3mol��5=0.5?mol��
�ʴ�Ϊ��0.5mol��
���������
�����Ѷȣ�һ��
3������� ������ѧ֪ʶ���ش��������⣺
��1��д�����ʳ��ˮ�Ļ�ѧ����ʽ������˫���ű������ת�Ƶķ������Ŀ��______�÷�Ӧ��������Ϊ______����ԭ��Ϊ______��
��2��Ư�۵���Ч�ɷ��ǣ��ѧʽ��______��Ư������ˮ���ܿ����е�CO2���ã���������Ư�ס�ɱ�����õĴ����ᣬ��ѧ��Ӧ����Ϊ______��
�ο��𰸣���1�����ʳ��ˮʱ�������������ӷŵ����������������������ӷŵ�����������ͬʱ�����������ƣ�

���õ��ӻ��ϼ۽��͵�������ˮ������ˮ����������ʧ���ӻ��ϼ����ߵ��������Ȼ��ƣ������Ȼ����ǻ�ԭ����
�ʴ�Ϊ��

��ˮ���Ȼ��ƣ�
��2��Ư�۵���Ч�ɷ���Ca��ClO��2��������ƺͶ�����̼��ˮ��Ӧ����̼��ƺʹ����ᣬ��Ӧ����ʽΪ
Ca��ClO��2+H2O+CO2�TCaCO3��+2HClO��
�ʴ�Ϊ��Ca��ClO��2��Ca��ClO��2+H2O+CO2�TCaCO3��+2HClO��
���������
�����Ѷȣ�һ��
4��ѡ���� ʵ����������FeSO4��Һʱ��Ϊ��ֹFeSO4�����������ʣ�������Һ�м��������ģ�������
A���
B������
C��������
D������
�ο��𰸣�A��п����FeSO4��Һ��Ӧ��������Һʧ�ܣ���A��ѡ��
B����������FeSO4��Һ����Ӧ���ҿɷ�ֹ�������ӱ����������ʣ���Bѡ��
C����������������������Ӧ�����������������ӣ���C��ѡ��
D�����������������ӣ��Ҳ��ܷ�ֹ�������ӱ���������D��ѡ��
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� ����˵����ȷ����
[? ]
A.������ԭ��Ӧ�ı�����Ԫ�ػ��ϼ۷����仯
B.��ԭ����һ���ܹ��õ����ӵ�����
C.��������Ԫ�ػ��ϼ����ߵķ�Ӧ�ǻ�ԭ��Ӧ
D.������Ӧ�ͻ�ԭ��Ӧ��ͬʱ������
�ο��𰸣�D
���������
�����Ѷȣ���