��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� &nb��Դ��www.91exam.orgsp;(12�֣�
��������һ����Ҫ�����ȼ�ϣ����������������������Գ��������ƻ����á���ҵ�Ͽ�����ú���������ˮú�����ϳɶ����ѡ���ش��������⣺
(1)����ˮú���ϳɶ����ѵ��ܷ�ӦΪ��
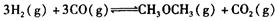 ?
?
�����Է�Ϊ��������Ӧ�ֱ����£�
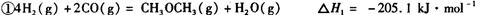
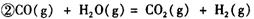
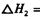 ��__________________ ______________
��__________________ ______________
(2)��һ�������µ��ܱ������У����ܷ�Ӧ�ﵽƽ�⣬ֻ�ı�һ��������ͬʱ��߷�Ӧ�ٺ�CO��ת���ʵ���_______(����ĸ���ţ���
a.�����¶�?b.���˴���?c.��С�������
d.����H2��Ũ��?e.����CO��Ũ��
(3)��һ����ɱ���ܱ������г��� ����һ���¶Ⱥ�ѹǿ�·�����Ӧ��
����һ���¶Ⱥ�ѹǿ�·�����Ӧ��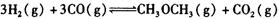 ����һ��ʱ��ﵽƽ�⣬�����ƽ��ʱ��������ܶ���ͬ��ͬѹ����ʼʱ��1.6�����ʣ��ٷ�Ӧ��ʼʱ�����淴Ӧ����
����һ��ʱ��ﵽƽ�⣬�����ƽ��ʱ��������ܶ���ͬ��ͬѹ����ʼʱ��1.6�����ʣ��ٷ�Ӧ��ʼʱ�����淴Ӧ���� �Ĵ�С��V(����____V���棩��� >������ < ����"="),�����ǣ�________________________________
�Ĵ�С��V(����____V���棩��� >������ < ����"="),�����ǣ�________________________________
��ƽ��ʱ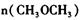 =_________________��ƽ��ʱCO��ת����= _________________��
=_________________��ƽ��ʱCO��ת����= _________________��
�ο��𰸣���12�֣�

�����������
�����Ѷȣ�һ��
2��ѡ���� ����ƽ����ϵ��mA������+ nB������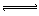 pC������+qD������+ Q�������жϣ�������ȷ����?
pC������+qD������+ Q�������жϣ�������ȷ����?
A�����¶Ȳ��䣬���������������1������ʱA��Ũ�ȱ�Ϊԭ����0.48������m+ n�� p+ q
B����ƽ��ʱ��A��B��ת������ȣ�˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm��n
C����ƽ����ϵ��������a mol���������м���b mol B�������´ﵽƽ��ʱ������������ʵ������ڣ�a+b������m+n=p+q
D���¶Ȳ���ʱ����ѹǿ������ԭ����2�����ﵽ��ƽ��ʱ��
�ο��𰸣�B��C
���������A���������1������ѹǿ��Ϊԭ����1��2��A��Ũ�ȱ�Ϊԭ����0.48����A��Ũ�ȼ�С�ˣ���ƽ��������Ӧ�����ƶ��ˣ�֤������Ӧ��һ�������������ķ�Ӧ����m��n��p��q��
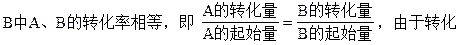
��֮�ȵ��ڷ���ʽ��ϵ���ȣ�����ʼ��Ӧ������ʵ���֮��ҲӦ����ϵ���ȡ�
C����ƽ����ϵ�м���b mol B�����´�ƽ��ʱ���������ʵ���û����Ϊ(a��b)mol��֤���÷�Ӧ��һ��������ķ�Ӧ����(m��n)��p��q��
D����m��n�� p��q����ѹǿ����ԭ����2��ʱ����ƽ��ʱ��������պ�Ϊԭ����� 1��2���� A��D��˵���Ǵ���ģ�B��C����ȷ�ġ�
�����Ѷȣ�һ��
3��ѡ���� ��һ����ɱ���ܱ������У�����һ������X��Y��������ӦmX��g�� nY��g������H =QkJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ��
nY��g������H =QkJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ��
 ? ?
�¶ȡ�
| 1
| 2
| 3
|
100
| 1.00
| 0.75
| 0.53
|
200
| 1.20
| 0.09
| 0.63
|
300
| 1.30
| 1.00
| 0.70
|
����˵����ȷ����
A.m��n? B. �¶Ȳ��䣬ѹǿ����Y��������������
C. Q��0?D.������䣬�¶����ߣ�ƽ�����淴Ӧ�����ƶ�
�ο��𰸣�B
������������ݱ������ݿ�֪���������ͬ�������£��¶�Խ��Y�����ʵ���Ũ��Խ����˵�������¶�������Y�����ɣ��������Ӧ�����ȷ�Ӧ����Q��0�����¶���ͬ�������£���������Խ��Y�����ʵ���Ũ��ԽС����˵������ѹǿ��������Y�����ɣ�������Ӧ���������Ŀ��淴Ӧ������m��n�����ѡ��ACD���Ǵ���ģ���ѡB��
�������������е��Ѷȵ����⣬�����ۺ���ǿ����ע�ض�ѧ������֪ʶ���̺�ϵ�е�ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ����ּ������ѧ��������û���֪ʶ���ʵ������������������ڵ���ѧ����ѧϰ��Ȥ������ѧ����ѧϰ��֪����
�����Ѷȣ���
4������� ��10�֣�(1)һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�(����ΪCu2O/ZnO)��? CO(g)��2H2(g) CH3OH(g)��
CH3OH(g)��
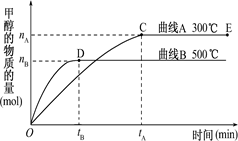
�������������ͼ��������и��⣺
�ٷ�Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK��?��
�������¶ȣ�Kֵ??(�������С�����䡱)
��2��һ���¶��£���3 mol A�����1 mol B����ͨ��һ�ܱ������У��������·�Ӧ��3A(g) + B(g) xC(g) ����д���пհף�����������̶�Ϊ2 L����Ӧ2 minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
xC(g) ����д���пհף�����������̶�Ϊ2 L����Ӧ2 minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
��x=?
��ƽ�������У�C���������Ϊ50%����B��ת������______________��
��3�����û�ѧ��Ӧԭ���о��������ȵ��ʼ��仯����ķ�Ӧ����Ҫ���塣��������Ѱ����ʵĴ����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4ClΪ�������Һ��������ȼ�յ��,�ŵ�����У���Һ��笠�����Ũ����������д���õ�ص�������Ӧʽ?��
�ο��𰸣���10�֣���1����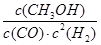 ���ڼ�С
���ڼ�С
��2���� 2?��66.7��?��3��N2+8H++6e��=2NH4+
�����������1���ٻ�ѧ��������һ�������µĿ��淴Ӧ�У������淴Ӧ��Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�ķ���ʽ��֪���÷�Ӧ��ƽ�ⳣ������ʽ��K��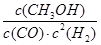 ��
��
�ڸ���ͼ���֪���¶�Խ�ߣ��״��ĺ���Խ�͡�˵�������¶ȣ�ƽ�����淴Ӧ����Խ�ͣ�������Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ�Kֵ��С��
��2����?3A(g) + B(g) xC(g)
xC(g)
��ʼŨ�ȣ�mol/L��? 1.5? 0.5? 0
ת��Ũ�ȣ�mol/L��?0.6? 0.2? 0.2x
2minʱŨ�ȣ�mol/L��? 0.9? 0.3? 0.2x
���Ը��������֪2x��0.4 mol/L
����x��2
��? 3A(g) + B(g) 2C(g)
2C(g)
��ʼŨ�ȣ�mol/L��? 1.5? 0.5? 0
ת��Ũ�ȣ�mol/L��? 3y? y? 2y
ƽ��Ũ�ȣ�mol/L��?1.5��3y? 0.5��y? 2y
���Ը��������֪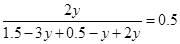
���y��1/3
����B��ת������1/3��0.5��66.67��
��3��ԭ����и���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�����Ե���������ͨ�롣����Ϊ�������Һ�����ԣ����������缫��Ӧʽ��N2+8H++6e��=2NH4+��
�������ڽ��п��淴Ӧ���йؼ���ʱ��һ����á�����ʽ�����У����ֱ��г���ʼ����ת������ƽ������ij��̵�����Ȼ��������֪������ʽ���㼴�ɡ�
�����Ѷȣ�һ��
5��ѡ���� ������ʵ��������������ԭ�����͵��ǣ�?��
���Ȼ�����Һ�����������յò����Ȼ�������
�����ڳ�ʪ�Ŀ�������������
��ʵ���ҿ����ű���ʳ��ˮ�ķ����ռ�����
�ܳ����£���1 mL pH��3�Ĵ����ˮϡ����100 mL�������pH��5
�������Ȼ��ع����Ʊ��أ�Na(l)��KCl(l)  K(g)��NaCl(l)
K(g)��NaCl(l)
����������������������ƽ����ϵ����ѹ����ɫ����
A���٢ڢ�
B���ڢ�
C���٢ۢܢ�
D���ڢݢ�
�ο��𰸣�B
����������ڲ��ǻ�ѧƽ�⣻��ƽ����ƶ�Ӧʹ��ɫ��dz����ɫ�����������С��Ũ�ȱ����ɵġ�
�����Ѷȣ�һ��