|
高考化学知识点总结《酯》试题特训(2017年最新版)(六)
2017-08-26 01:53:34
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 I.乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的结构简式为____________。
(2)下列物质中,不可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3
B.CH3CHCl2
C.CH3CH2OH
D.CH3CH2Br
| (3)已知 2CH3CHO+O2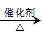 ?2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。 ?2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
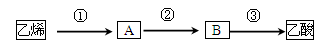
反应②的化学方程式为____________________________________。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________________,反应类型是__________________。
II.在实验室可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。
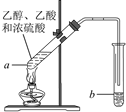
(1)乙醇、乙酸分子中官能团的名称分别是_________、_________。
(2)试管a中发生反应的化学方程式为
_____________________________________________,
反应类型是______________。
(3)浓H2SO4的作用是:__________________________。
反应开始前,试管b中盛放的溶液是____________。
该溶液的作用是?
___________________________________________________________________________________。
参考答案:I. (1)H2C=CH2?(2)B
(3)2CH3CH2OH+O2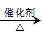 ?2CH3CHO+2H2O ?2CH3CHO+2H2O
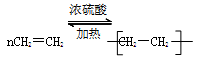 ?加聚反应 ?加聚反应
II.? (1)羟基、羧基
(2)CH3COOH+C2H5OH CH3COOC2H5+H2O? 酯化反应
(3)催化剂、吸水剂
(4)饱和碳酸钠溶液
吸收乙醇、中和乙酸,便于闻酯的气味;降低酯的溶解度,利于分层析出 (3分)
本题解析:I.(1)乙烯的结构简式为H2C=CH2。(2)A、乙烯和氢气加成生成CH3CH3,C、乙烯和水加成生成CH3CH2OH,? D、乙烯与溴化氢加成生成CH3CH2Br,选B;(3)由题给流程图知,反应②为乙醇催化氧化生成乙醛,化学方程式为2CH3CH2OH+O2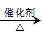 2CH3CHO+2H2O。 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为 2CH3CHO+2H2O。 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为
 ,反应类型是加聚反应。II.(1)乙醇、乙酸分子中官能团的名 ,反应类型是加聚反应。II.(1)乙醇、乙酸分子中官能团的名
称分别是羟基、羧基;(2)试管a中乙酸与乙醇发生酯化反应生成乙酸乙酯,化学方程式为CH3COOH+C2H5OH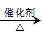 CH3COOC2H5+H2O,反应类型是酯化反应。(3)浓H2SO4的作用是:催化剂、吸水剂;(4)反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液;该溶液的作用是吸收乙醇、中和乙酸,便于闻酯的气味;降低酯的溶解度,利于分层析出。 CH3COOC2H5+H2O,反应类型是酯化反应。(3)浓H2SO4的作用是:催化剂、吸水剂;(4)反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液;该溶液的作用是吸收乙醇、中和乙酸,便于闻酯的气味;降低酯的溶解度,利于分层析出。
本题难度:一般
2、选择题 醋酸酐的结构简式为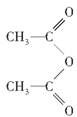 ,1 mol醋酸酐与1 mol水反应,可得2 mol醋酸。某饱和一元醇A 7g跟醋酸酐反应,生成醋酸某酯7.9g,反应后回收到1.2g A,则A的相对分子质量为( ) ,1 mol醋酸酐与1 mol水反应,可得2 mol醋酸。某饱和一元醇A 7g跟醋酸酐反应,生成醋酸某酯7.9g,反应后回收到1.2g A,则A的相对分子质量为( )
A.98
B.116
C.158
D.102
参考答案:B
本题解析:设醇A的相对分子质量为M,由关系式
ROH~CH3COOR
M M+42
(7g-1.2g) 7.9g
M:(M+42)=(7g-1.2g) ∶7.9g,
M=116。
本题难度:一般
3、实验题 某课外小组设计的实验室制取乙酸乙酯的装置(如图所示),A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。按图连接装置,用酒精灯对烧瓶B加热,当观察到D中有明显现象时停止实验。试完成下列问题
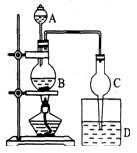
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是:_________。
(2)球形干燥管除起冷凝作用外,另一重要作用是_________________。
(3)装置D中饱和碳酸钠溶液的作用是___________________________
(4)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯??,原因是:?。
参考答案:

本题解析:略
本题难度:简单
4、选择题 下列有关物质分类中,全部正确的一组是
[? ]
A.CO(NH2)2 (无机物);NH4CNO(有机物); CH2=CHCH3 (脂肪烃)
B.CH3COCH3(醚);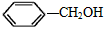 (醇)?; (醇)?;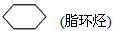
C.HOCOOH(羧酸) ;CH3OOCCOOCH3(酯) ;  (酚) (酚)
D.OHCCH3(醛);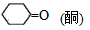 ;CCl3F(卤代烃) ;CCl3F(卤代烃)
参考答案:D
本题解析:
本题难度:简单
5、实验题 某化学小组以苯甲酸为原料制取苯甲酸甲酯。有关物质的沸点和相对分子质量如表:
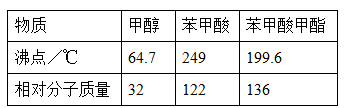
I.合成苯甲酸甲酯粗产品
在烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约0.79g/mL) ,再小心加入3mL 浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)该反应中浓硫酸的作用?,若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式?,甲醇过量的原因?。?
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是??。
(3)甲、乙、丙三位同学分别设计了如图三套实验室制取苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的特点,最好采用?装置(填“甲”、“乙”、“丙”)。

Ⅱ.粗产品的精制
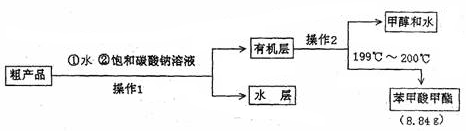
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程图进行精制,请根据流程图填入恰当操作方法的名称:操作I为?,操作II为?。
(5)以上流程图中加入Na2CO3溶液后,放入分液漏斗中振荡、静置,要得到有机层,其具体操作是?。
(6)苯甲酸甲酯的产率为?。
参考答案:(1)催化剂和吸水剂,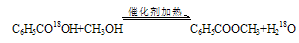 该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇的量,可提高产率 该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇的量,可提高产率
(2)冷却后补加
(3)乙
(4)分液;蒸馏
(5)将分液漏斗上口的玻璃塞打开(或使塞上的凹槽对准漏斗口上的小孔),再旋开分液漏斗活塞,用锥形瓶接收下层液体,待下层液体刚好流尽时关闭活塞,将有机层从分液漏斗上口倒入另一干净的容器(或烧杯)中
(6)65 %
本题解析:(1)甲醇和苯甲酸在浓硫酸作催化剂的条件下加热发生酯化反应得到苯甲酸甲酯和水。由于浓硫酸有吸水性,吸收反应产生的水,使酯化反应的平衡正向移动,可以提高反应物的转化率及产品的产率。所以在该反应中浓硫酸的作用是作催化剂和吸水剂。酯化反应的实质是酸脱羟基醇脱氢。所以该反应的化学方程式为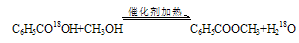 。甲醇要过量是因为该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇的量,可提高产率。(2)如果加热一段时间后发现忘记加碎瓷片,应该停止加热,冷却至室温,后再补加。 。甲醇要过量是因为该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇的量,可提高产率。(2)如果加热一段时间后发现忘记加碎瓷片,应该停止加热,冷却至室温,后再补加。
(3)甲虽然采用了冷却装置,但甲醇已经脱离了反应体系,对提高反应物的利用率不利,丙没有冷却降温装置,会导致一部分反应物及产物挥发逸出,无论是对环境还是对产品的制取都不利。而乙把甲、丙的优点集结在一起,既减少了反应物的挥发消耗,也提高了产品的产率。故选择乙装置。
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,先加入水可以溶解硫酸,再加入饱和的Na2CO3溶液,既可以反应消耗苯甲酸,也可以降低苯甲酸甲酯的溶解度。由于它们是互补相容的液体,因此可常用分液的方法分离。在分液得到的有机物中因为甲醇与苯甲酸甲酯的沸点不同,将它们通过蒸馏分离开来。
(5)分液的具体操作是:将分液漏斗上口的玻璃塞打开(或使塞上的凹槽对准漏斗口上的小孔),再旋开分液漏斗活塞,用锥形瓶接收下层液体,待下层液体刚好流尽时关闭活塞,将有机层从分液漏斗上口倒入另一干净的容器(或烧杯)中。
(6)n(苯甲酸)="m/M=12.2g" ÷122g/mol=0.1mol;n(甲醇)=(20×0.79g) ÷32g/mol="15.8g÷32g/mol" =0.494mol。苯甲酸的物质的量不足,应该以苯甲酸为标准来进行计算。n(苯甲酸甲酯)=" m/M=8.84g÷" 136g/mol="0.065mol." 苯甲酸甲酯的产率为(0.065mol÷0.1mol)×100%="65" %
本题难度:一般
| 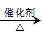 ?2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
?2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
