微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是

A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
参考答案:B
本题解析:A、K1闭合构成原电池,铁棒是负极,铁失去电子,铁棒上发生的反应为Fe+2e-→Fe2+,A不正确;B、K1闭合构成原电池,铁棒是负极,铁失去电子,石墨棒是正极,溶液中的氧气得到电子转化为OH-,石墨棒周围溶液pH逐渐升高,B正确;C、K2闭合构成电解池,铁棒与电源的负极相连,作阴极不会被腐蚀,属于外加电流的阴极保护法,C不正确;D、K2闭合构成电解池,铁棒与电源的负极相连,作阴极溶液中的氢离子放电生成氢气。石墨棒是阳极,溶液中的氯离子放电生成氯气,电路中通过0.002NA个电子时,两极均产生0.001mol气体,共计是0.002mol气体,D不正确,答案选B。
本题难度:一般
2、选择题 下列各组实验装置能达到实验目的是( )
A.用图1所示装置组成锌铜原电池
B.用图2所示装置在铁棒上镀锌
C.用图3所示装置测定稀硫酸和稀NaOH反应的中和热
D.用图4所示装置研究温度对2NO2(g)?N2O4(g)平衡的影响
参考答案:A.含有盐桥的原电池中,电极材料和电解质溶液中金属离子必须是相同元素,该图中金属材料和电解质溶液中金属阳离子不是相同元素,所以不能构成原电池,故A错误;
B.在铁棒上镀锌时,锌作阳极,铁棒作阴极,故B错误;
C.缺少玻璃搅拌棒,如果不搅拌溶液会导致溶液温度不均匀,测量中和热不准确,故C错误;
D.二氧化氮是红棕色气体,四氧化二氮是无色气体,在同一反应装置的可逆反应中,根据温度不同导致气体颜色的不同确定温度对可逆反应的影响,故D正确;
故选D.
本题解析:
本题难度:简单
3、填空题 用铜、银与硝酸银设计一个原电池,此电池的负极是:______,负极的电极反应式是:______总反应方程式为______.
参考答案:根据金属的活泼性判断,铜作负极,铜失去电子变成离子进入溶液,发生氧化反应,Cu-2 e-=Cu2+;银作正极,银离子得电子生成银单质,发生还原反应,2Ag++2 e-=2Ag;两个电极反应式相加即得总反应方程式,Cu+2Ag+=2Ag+Cu2+.故答案为:Cu;? Cu-2 e-=Cu2+;Cu+2Ag+=2Ag+Cu2+
本题解析:
本题难度:一般
4、填空题 根据如图所示的装置回答下列问题:?
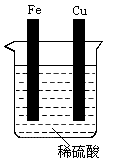
(1)铁片与铜片不用导线连接,有何现象发生?写出反应的化学方程式__________。
(2)用导线把金属片连接起来,现象有什么不同?用最恰当的化学方程式表示发生的反应__________。
参考答案:(1)铁片与铜片不用导线连接,则铁片表面有气泡产生,但速率较慢。 Fe +H2SO4=FeSO4 +H2↑
(2)①气泡不从铁片表面而是从铜片表面逸出;②产生氢气的速率明显加快。电极反应式:
负极:Fe-2e-=Fe2+?
正极:2H++2e-=H2↑。
本题解析:
本题难度:一般
5、简答题 请画出电解氯化铜溶液的电解装置图.另外在图中注明电解质材料及电极名称,标出电子流动方向,并写出各电极反应式.
______极反应式:______
______极反应式:______.
参考答案:电解氯化铜溶液时,阳极发生失电子的氧化反应,电极反应为:2Cl--2e-=Cl2↑,阴极发生得电子的还原反应,电极反应为:Cu2++2e-→Cu,电解装置的构成条件:有电解质溶液氯化铜,闭合回路,两个电极,装置以及电子流动方向和各电极反应式如下:

,故答案为:阳;2Cl-→Cl2↑+2e-;阴;Cu2++2e-→Cu;

.
本题解析:
本题难度:一般