微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)微粒X2-核外有18个电子,该离子的结构示意图?。
(2)由1H216O与2H217O所代表的物质中,共有?种元素,?种原子,16O、17O的关系为?。
(3)已知:碳元素有12C、13C、14C;氧元素有16O、17O、18O,则它们能够形成?种CO2分子。
参考答案:(1) ⑵2,4,同位素? ⑶? 18?;
⑵2,4,同位素? ⑶? 18?;
本题解析:(1)X2-核外有18个电子,带两个单位的负电荷,则该微粒的质子数为16;(2)同种元素用同一符号表示,不同的核素表示不同的原子;(3)CO2由一个碳原子和两个氧原子构成,碳、氧均有三种核素,两个氧原子可为同一核素,也可为不同核素,故总共有18种组合。
点评:对化学用语的考查是高考必考知识点,难度不大,考生在平时的学习过程中应注意化学用语的规范使用。
本题难度:一般
2、填空题 (16分)某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁。其生产工艺流程如下:

已知:
①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-:
②)TiOSO4水解的反应为:TiOSO4+(x+1)H2O=TiO2?xH2O↓+H2SO4
请回答:
(1)步骤①所得滤渣的主要成分为__________________。
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比_______。
(3)步骤④需控制反应温度低于35℃,其目的是___________________。
(4)步骤④反应的离子方程式是______________________。
(5)已知:FeCO3(s)  Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因__________。
Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因__________。
(6)溶液B常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为_____________________________________。
(7)Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的_________(填“深”或“浅”),其原因是______________。
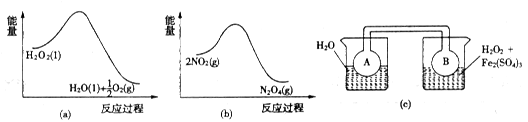
参考答案:(16分) (1)TiO2?xH2O、Fe(2分);(2)1:4 (2分)(3)防止NH4HCO3分解(或减少Fe2+的水解)(2分)
(4)Fe2+ + 2HCO3一="=" FeCO3 ↓+ H2O + CO2 ↑(2分)
(5)乳酸(电离出的H+)与CO32一反应,降低了CO32一的浓度,使上述沉淀溶解平衡正向移动,使碳酸亚铁溶解得到乳酸亚铁溶液(2分)
(6)2SO42--2e-==S2O82-(2分)
(7)①深(2分);②H2O2分解放热,使平衡2NO2 N2O4向生成NO2方向移动(2分)
N2O4向生成NO2方向移动(2分)
本题解析:(1)在反应废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,向其中加入Fe屑,发生反应:Fe2(SO4)3+Fe= 3FeSO4; Fe+H2SO4= FeSO4+ H2↑; 随着反应的进行,溶液的酸性减弱,TiOSO4发生水解反应: TiOSO4+(x+1)H2O=TiO2?xH2O↓+H2SO4;所以得到的滤渣成分是TiO2?xH2O;(2) ③FeSO4溶液蒸发浓缩,冷却结晶得到绿矾,然后将其在空气中煅烧,发生反应:4FeSO4+O2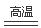 2Fe2O3+4SO3,生成铁红和三氧化硫,该反应中氧化剂是O2,还原剂是FeSO4。由于在氧化还原反应中电子转移守恒,所以氧化剂与还原剂的物质的量之比1:4;(3)步骤④是FeSO4溶液中加入NH4HCO3,来制取FeCO3,需控制反应温度低于35℃,是为了防止NH4HCO3分解及减少Fe2+的水解反应的发生;(4)步骤④反应的离子方程式是Fe2+ + 2HCO3一="=" FeCO3 ↓+ H2O + CO2 ↑;(5) FeCO3难溶于水,但是在水中也有一定的溶解度,因此在溶液中存在沉淀溶解平衡:FeCO3(s)
2Fe2O3+4SO3,生成铁红和三氧化硫,该反应中氧化剂是O2,还原剂是FeSO4。由于在氧化还原反应中电子转移守恒,所以氧化剂与还原剂的物质的量之比1:4;(3)步骤④是FeSO4溶液中加入NH4HCO3,来制取FeCO3,需控制反应温度低于35℃,是为了防止NH4HCO3分解及减少Fe2+的水解反应的发生;(4)步骤④反应的离子方程式是Fe2+ + 2HCO3一="=" FeCO3 ↓+ H2O + CO2 ↑;(5) FeCO3难溶于水,但是在水中也有一定的溶解度,因此在溶液中存在沉淀溶解平衡:FeCO3(s)  Fe2+(aq)+CO32-(aq),当向其中加入乳酸时,乳酸电离出的H+与CO32一反应,形成HCO3-,降低了CO32一的浓度,使上述沉淀溶解平衡正向移动,使碳酸亚铁溶解得到乳酸亚铁溶液;(6)在溶液B中含有SO42一,常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生氧化反应,该电极的电极反应可表示为2SO42--2e-==S2O82-;(7)根据图a可知H2O2的负极反应是放热反应,反应2NO2
Fe2+(aq)+CO32-(aq),当向其中加入乳酸时,乳酸电离出的H+与CO32一反应,形成HCO3-,降低了CO32一的浓度,使上述沉淀溶解平衡正向移动,使碳酸亚铁溶解得到乳酸亚铁溶液;(6)在溶液B中含有SO42一,常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生氧化反应,该电极的电极反应可表示为2SO42--2e-==S2O82-;(7)根据图a可知H2O2的负极反应是放热反应,反应2NO2 N2O4的正反应是放热反应。在装置c的左边烧内放有水,在右边的烧杯内放有H2O2和Fe2(SO4)3的混合溶液,因为Fe3+对H2O2的分解具有催化作用,所以H2O2会不断分解,放出热量没事右边的烧杯内的水的温度升高。根据平衡移动原理:升高温度,平衡向吸热的逆反应方向移动,NO2浓度增大,所以连通器内的气体颜色加深。
N2O4的正反应是放热反应。在装置c的左边烧内放有水,在右边的烧杯内放有H2O2和Fe2(SO4)3的混合溶液,因为Fe3+对H2O2的分解具有催化作用,所以H2O2会不断分解,放出热量没事右边的烧杯内的水的温度升高。根据平衡移动原理:升高温度,平衡向吸热的逆反应方向移动,NO2浓度增大,所以连通器内的气体颜色加深。
考点:考查生产钛白粉产生的废液的综合利用的知识。主要包括物质的分离、氧化还原反应中物质的关系、盐的水解、沉淀溶解平衡、原电池反应原理、反应热的综合利用及温度对可逆反应的平衡移动的影响。
本题难度:困难
3、选择题 下列说法正确的是?
A.c(H+)=0.1mol/L的甲酸溶液中,HCOO-和H+数目之和为0.1 NA
B.通常情况下,溴是液态,碘是固态,所以I―I键比Br-Br弱
C.将稀氨水逐滴加入稀硫酸中,当溶液pH =7时,2C(NH4+)=C(SO42-)
D.合成顺丁橡胶( )的单体是CH2=CH―CH=CH2
)的单体是CH2=CH―CH=CH2
参考答案:D
本题解析:
正确答案D
A.不正确,c(H+)=0.1mol/L的甲酸溶液中,HCOO-和H+数目之和,没有体积,不好计算;
B.不正确,通常情况下,溴是液态,碘是固态,是因为I2的相对分子质量大于Br2;
C.不正确,将稀氨水逐滴加入稀硫酸中,当溶液pH =7时,根据电荷守恒应为: C(NH4+)=2C(SO42-)
D.正确
本题难度:一般
4、选择题 用高铁酸钠(Na2FeO4)对湖水消毒,是城市饮水处理的新技术。已知反应Fe2O3 + 3Na2O2="=2" Na2FeO4?+? Na2O .下列说法正确的是
A.Na2O2既是氧化剂又是还原剂
B.Na2FeO4既是氧化产物又是还原产物
C.3摩尔Na2O2发生反应,有12摩尔电子转移
D.在Na2FeO4中Fe为+4价,只有强氧化性,能消毒杀菌
参考答案:B
本题解析:略
本题难度:一般
5、选择题 下列化学用语书写正确的是(?)
A.次氯酸的结构式:H-Cl-O
B.氯化镁的电子式:
C.作为相对原子质量测定标准的碳核素: 614C
D.用电子式表示氯化氢分子的形成过程:
参考答案:B
本题解析:次氯酸的结构式是H-O-Cl,A不正确;作为相对原子质量测定标准的碳核素是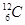 ,选项C不正确;氯化氢是共价化合物,D不正确,应该是
,选项C不正确;氯化氢是共价化合物,D不正确,应该是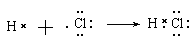 ,答案选B。
,答案选B。
点评:该题是中等难度的试题,也是高考中的常见题型与重要的考点。该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度。该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住,并能灵活运用。
本题难度:一般