微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某同学一次实验中需称取5.0gNaOH用于配置一定体积一定浓度的NaOH溶液,下列操作对所配制溶液浓度无影响的是
[? ]
A.所用NaOH已经潮解
B.容量瓶未干燥就使用
C.转移溶液后未洗涤
D.称量时误用“左码右物”
参考答案:BD
本题解析:
本题难度:简单
2、简答题 实验室需要0.1mol?L-1NaOH溶液450mL和0.5mol?L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是______(填仪器名称).
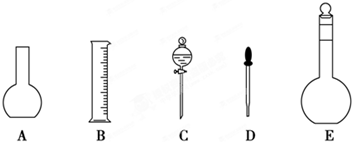
(2)容量瓶不能用于______(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为______g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度______0.1mol?L-1(填“大于”“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度______0.1mol?L-1.
(4)根据计算得知,所需质量分数为98%、密度为1.84g?cm-3的浓硫酸的体积为______mL(计算结果保留一位小数).如果实验室有15mL、20mL、50mL量筒,应选用______mL量筒最好.配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______.
参考答案:(1)用容量瓶配制溶液,用胶头滴管定容;还需要用到的仪器有:溶解或稀释药品的烧杯、搅拌或引流用的玻璃棒,
故答案为:AC;烧杯和玻璃棒;
(2)容量瓶只能用来配制一定体积准确浓度的溶液,不能配制或测量容量瓶规格以下的任意体积的液体,不能稀释或溶解药品,不能用来加热溶解固体溶质,故选BCF;
(3)m=CVM=0.1mol/L×0.5L×40g/mol=2.0g,若定容时仰视刻度线,溶液的体积偏大,则所得溶液浓度小于0.1mol?L-1,若NaOH溶液在转移至容量瓶时,洒落了少许,溶质的物质的量偏小,则所得溶液浓度 小于0.1mol?L-1,
故答案为:2.0;小于;小于;
(4)浓硫酸的浓度=C=103ρwM=103×1.84×98%98mol/L=18.4mol/L,浓硫酸稀释前后溶质的物质的量不变,设浓硫酸的体积为V,所以18.4mol/L×V=0.5/L×0.5L,V=0.0136L=13.6mL,选取的量筒规格应该等于或大于量取溶液体积,故选15mL量筒,稀释浓硫酸的正确操作是:将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌,防止液体溅出,
故答案为:13.6;15;将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌.
本题解析:
本题难度:一般
3、选择题 配制100mL?1.0mol?L-1的Na2CO3溶液,下列情况会导致溶液浓度偏高的是( )
A.容量瓶使用前用1.0?mol?L-1的Na2CO3溶液润洗
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.仰视确定凹液面与刻度线相切
D.用敞口容器称量Na2CO3且时间过长
参考答案:A
本题解析:
本题难度:一般
4、选择题 已知氯化铁溶液中通入硫化氢可发生反应:2FeCl3+H2S→2FeCl2+S↓+2HCl.在标准状况下,向100mLFeCl3溶液中通入a?L的H2S气体恰好反应后,再加入足量的铁粉充分反应.所得溶液经测定金属阳离子的浓度为3mol/L,若反应过程中溶液体积不变,则原FeCl3溶液的物质的量浓度为
A.1.5mol/L
B.2?mol/L
C.1?mol/L
D.无法确定
参考答案:B
本题解析:分析:该反应过程为:氯化铁和硫化氢反应生成氯化亚铁和盐酸,盐酸再和铁反应生成氯化亚铁,所以反应实质是氯化铁和铁反应生成氯化亚铁,根据氯原子守恒计算氯化铁的物质的量浓度.
解答:该反应过程为:氯化铁和硫化氢反应生成氯化亚铁和盐酸,盐酸再和铁反应生成氯化亚铁,所以反应实质是氯化铁和铁反应生成氯化亚铁,根据氯原子守恒计算氯化铁的物质的量浓度,
2FeCl3+Fe=3FeCl2,根据方程式知,c(FeCl3)=c(FeCl2)× =3mol/L×
=3mol/L× =2mol/L,
=2mol/L,
故选B.
点评:本题考查了物质的量的有关计算,明确反应实质是解本题关键,然后利用原子守恒进行分析解答即可,难度不大.
本题难度:困难
5、选择题 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为cmol/L,则下列关系中不正确的是
A.ρ=
B.ω=
C.ω=
D.c=
E.c=
参考答案:A
本题解析:分析:A、由表达式可知,该密度=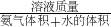 ,溶液体积不等于氨气体积与水的体积之和;
,溶液体积不等于氨气体积与水的体积之和;
B、根据c=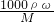 进行计算;
进行计算;
C、根据n= 计算氨气的物质的量,根据m=nM计算氨气的质量,利用m=ρV计算水的质量,根据溶质质量分数=
计算氨气的物质的量,根据m=nM计算氨气的质量,利用m=ρV计算水的质量,根据溶质质量分数= ×100%计算
×100%计算
D、根据c=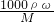 计算.
计算.
解答:A、由表达式可知,该密度=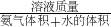 ,溶液体积不等于氨气体积与水的体积之和,故A错误;
,溶液体积不等于氨气体积与水的体积之和,故A错误;
B、由c=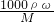 可知,该溶液氨气质量分数ω=
可知,该溶液氨气质量分数ω= ,故B正确;
,故B正确;
C、氨气的物质的量为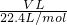 =
=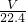 mol,故氨气的质量为
mol,故氨气的质量为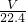 mol×17g/mol=
mol×17g/mol=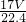 g,1L水的质量为1000g,故该溶液的质量分数为ω=
g,1L水的质量为1000g,故该溶液的质量分数为ω=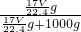 ×100%=
×100%=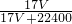 ,故C正确;
,故C正确;
D、由C可知质量分数为ω=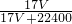 ,故c=
,故c=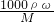 =
=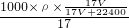 =
=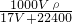 ,故D正确;
,故D正确;
故选A.
点评:考查质量分数、物质的量浓度的有关计算,难度中等,注意公式的理解与灵活运用,题目为字母型计算,计算量较大,需要学生细心观察进行计算.
本题难度:一般