微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3++4NH3・H2O=AlO2-+4NH4++2H2O
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
D.在溴化亚铁溶液中通入过量的氯气:Cl2+2Fe2++2Br-=2Fe2++2Cl-+Br2
参考答案:
B
本题解析:
一般来说微溶物作为反应物且为澄清溶液时,写成离子形式;C中三价铁与碘离子发生氧化还原反应。
本题难度:一般
2、选择题 下列离子方程式正确的是?(?)
A.二氧化硅与强碱溶液反应: SiO2 +2OH - = SiO32-+ H2O
B.将氯气通入NaOH溶液中:Cl2 + OH -= Cl-+ HClO
C.金属钠与水反应:Na+2H2O=Na+ + 2OH - + H2↑
D.少量的金属锌加入到FeCl3溶液中: 2Fe3++3Zn = 2Fe+3Zn2+
参考答案:A
本题解析:A正确。
B错误,正确的应该是Cl2 + 2OH -= Cl-?+ ClO-+H2O
C错误,元素不守恒,正确的应该是 2Na+2H2O=2Na+ + 2OH - + H2↑
D错误,不符合反应事实,Zn不能将+3价铁离子还原成铁单质。
本题难度:一般
3、选择题 下列离子方程式中,正确的是
[? ]
A.NaAlO2溶液中通入少量二氧化碳:AlO2-+ CO2 + 2H2O = Al(OH)3↓+ HCO3-
B.高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+ 5C2O42-+ 16H+ = 2Mn2+ + 10CO2↑+ 8H2O
C.用稀硫酸除去铁片表面的铁锈:FeO + 2H+ = Fe2+ + H2O
D.用惰性电极电解饱和食盐水:2Cl- + 2H2O Cl2↑ + H2↑ + 2OH-
Cl2↑ + H2↑ + 2OH-
参考答案:D
本题解析:
本题难度:一般
4、填空题 (10分)有A、B、C、D、E五种微粒,其组成均有氢元素,且电子总数为10个,A是双原子的阴离子,它们之间能发生下列变化:
(1)A+B C+D↑? (2)C+C
C+D↑? (2)C+C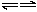 A+E? (3)D+E
A+E? (3)D+E B+C
B+C
由此可知它们的化学式分别为:
A?,B?,
C?,D?,E?。
参考答案:A?OH-,B?NH4+, C?H2O,DNH3,E?H3O+。
本题解析:
A:OH-、B:NH4+、C:H2O、D:NH3、、E:H3O+
A+B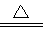 =C+D:NH4+ +OH-=△=NH3↑+H2O
=C+D:NH4+ +OH-=△=NH3↑+H2O
C+C =A+E:2H2O=H3O+ +OH-
=A+E:2H2O=H3O+ +OH-
D+E =B+C:NH3+H3O+=NH4+ +OH-
=B+C:NH3+H3O+=NH4+ +OH-
本题难度:一般
5、选择题 下列离子方程式书写正确的是( )
A.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO2-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓
B.铝片溶于NaOH溶液:Al+2OH-=AlO2-+H2↑
C.向1mol碘化亚铁的溶液中通入标准状况下22.4L氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.Fe3O4溶于稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O
参考答案:A、碳酸氢镁溶液中加入过量石灰水,碳酸氢根和镁离子全部反应,离子方程式中符合2:1,且镁离子形成的氢氧化镁溶解性更小,所以生成的是氢氧化镁沉淀,结合离子方程式的书写原则写出离子方程式为:Mg2++2HCO2-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓,故A正确;
B、不符合电荷守恒和反应实质,铝片溶于NaOH溶液在发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故B错误;
C、碘化亚铁的溶液中离子还原性Fe2+<I-,通入氯气先与I-反应2I-+Cl2=I2+2Cl-;1mol碘化亚铁中含I-2mol,1molFe2+,1molCl2氧化2molI-,所以只发生:2I-+Cl2=I2+2Cl-;故C错误;
D、Fe3O4溶于稀HNO3,硝酸具有强氧化性,生成产物中不能含有亚铁离子,故D错误;
故选A.
本题解析:
本题难度:一般