��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣��ù���Ч�Ķ������ȣ�ClO2�����Һ�Ƚ����������ɱ�����������彡���к����л��ȴ��
��1����ҵ�ϣ�ClO2����NaClO3��Na2SO3��Һ��ϲ��������ữ��Ӧ�Ƶã��ڸ÷�Ӧ��NaClO3��Na2SO3�����ʵ���֮��Ϊ? ��?��
��2����Ч�Ⱥ����Ǻ�����������һ����Ҫָ�꣬��Ч�Ⱥ����Ķ���Ϊ����HI����������ͬ����I2����Cl2��������ָ������������������֮�ȣ����ðٷ�����ʾ����ClO2����Ч�Ⱥ�����? ��?��
��3����ѧС���ͬѧ������ClO2������������ˮ������Ԫ�غ����IJⶨ���ٶ�ClO2ȫ��ת��ΪCl���������ǽ���������ʵ�飺��30.00 mLˮ���мӼ���K2CrO4��Һ��ָʾ������0.001000 mol��L��1 AgNO3��Һ�ζ�������ש��ɫAg2CrO4��������ʱ����ζ��յ㣬��ʱ��ȥAgNO3��Һ12.12 mL��
��ˮ����Cl�������ʵ���Ũ����? ��?��?
����֪Ksp(AgCl) = 1.78��10-10��Ksp(Ag2CrO4) = 2.00��10-12�����ڵζ��յ�ʱ�������Һ��CrO42����Ũ����5.000��10��3 mol��L��1 ���Լ����ʱ��Һ��Cl����Ũ���Ƕ��١�
���Լ����ʱ��Һ��Cl����Ũ���Ƕ��١�
�ο��𰸣���10�֡�
��1��2�U1��2�֣�?��2��263%����2.63����2�֣�
��3����4.04��10-4 mol��L��1��2�֣�
�ڵ�c(CrO42-) = 5.00��10-3 mol��L��1����ש��ɫ����ʱ��
��Ksp(Ag2CrO4)�� c(CrO42-)=5.00��10-3����c(Ag+) = 2.00��10-5 mol��L��1��2�֣�
���ԣ�c(Cl-) = 8.90��10-6 mol��L��1��2�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ���й�����ˮ�������У���ȷ����:?
A��������ˮ��û�з��ӣ�ֻ������
B��������ˮ�ڹ��յ������£����Բ������壬������������
C��������ˮ�еμ���������Һ��û���κ�����
D����������ʹʪ�����ɫ������ɫ
�ο��𰸣�D
���������������ˮ�ijɷּ�����
A����ˮ�д���ˮ�������ἰ�������ַ��ӣ���
B��Cl2��H2O=HCl��HClO? 2HClO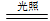 2HCl��O2�����ʸ�����Ϊ����
2HCl��O2�����ʸ�����Ϊ����
C����ˮ�е������ӿ������������ɰ�ɫ����
D����ˮ�еĴ��������ǿ�����ԡ�Ư���ԣ���ʹʪ�����ɫ������ɫ
�ʴ�ΪD
�����Ѷȣ���
3��ѡ���� �ձ���ʢ���������ʣ����ڷ���һ��ʱ�����Һ���������ӵ���
A��Ũ����
B��Ũ����
C��Ũ����
D��Ũ����
�ο��𰸣�B
������������ᡢ���ᡢ���ᶼ���ӷ��ģ����Գ��ڷ���һ��ʱ�����Һ�������С��Ũ���������ˮ�ԣ����ڷ���һ��ʱ�����Һ���������ӣ���ѡB��
�����������ǻ�����֪ʶ�Ŀ��飬�ѶȲ�����Ĺؼ���������ס���ᡢ���ᡢ�����Ũ��������ʣ�Ȼ��������������ü��ɡ�
�����Ѷȣ���
4������� ��13�֣�ʵ�������������������������з�����ȡ�ģ�
4HCl��Ũ����MnO2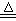 Cl2����MnCl2��2H2O
Cl2����MnCl2��2H2O
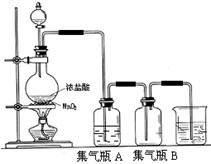
�Իش��������⣺
��1���÷�Ӧ��������ԭ��Ӧ��?�������������ԭ��Ӧ����ָ��?����������?�ǻ�ԭ����д���÷�Ӧ�����ӷ���ʽ?��
��2������ƿA��ʢװ���DZ���ʳ��ˮ��ע�������ڱ���ʳ��ˮ���ܽ�Ⱥ�С�����Ȼ����ڱ���ʳ��ˮ�е��ܽ����ܴ���������?��
��3����������ˮ�����ԣ��������ж������о��ҵĴ̼��ԣ�������������������ж���������������β��ֱ����������У�����Ⱦ������ʵ�����пɲ���?��Һ�������ж���������
��4��һ��ʵ���У���Ũ����80mL�����ܶ�Ϊ1.19g��cm-3��HCl����������Ϊ36.5%����MnO2ǡ����ȫ��Ӧ��������5.6L����״���£����������Լ���Ũ��������ʵ���Ũ�Ⱥͱ�������HCl�����ʵ�����
�ο��𰸣���ÿ��1�֣����ӷ���ʽ2�֣���������3�֣���1���ǣ�MnO2��Ũ���4H+��2Cl-��MnO2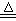 Cl2����Mn2+��2H2O��
Cl2����Mn2+��2H2O��
��2����ȥ�����л��е�HCl���壨3��Ũ�������ƣ�Ũ�
��4��Ũ��������ʵ���Ũ���ǣ�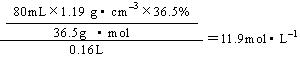
��������HCl�����ʵ���Ϊ��(5.6L/22.4L��mol-1)��2��0.5mol? (��ʾ���ɻ�ѧ��Ӧ����ʽ��֪���������������1mol�������ɣ�����2mol��HCl������)
�����������
�����Ѷȣ�һ��
5��ѡ���� ijѧ��������ˮ�����������ʵ���Һ�������������ҩƷ���ʵ��ǣ�?��?
A��ʯ��
B��������
C����������
D���Ȼ���
�ο��𰸣�D
�������������ˮһ����������������������ˮ���������Ժ�ǿ�����ԣ����ѡ��A��B��C���ǻᷢ���仯�ģ����Ȼ������ᷢ���仯����ѡD��
��������������ˮ���õ���ˮ����ˮ�д���H����OH����Cl����ClO����Cl2��HClO��H2O���ݴ˿����ж���ˮ���뷴Ӧʱ��������á�
�����Ѷȣ�һ��