微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定条件下,将等体积的NO和O2一同置于试管中,并将试管倒立于水中,充分反应后剩余气体约为原总体积的
[? ]
A.1/8?
B.1/4?
C.3/8?
D.3/4?
参考答案:A
本题解析:
本题难度:一般
2、选择题 将充有20mLN2和NO2混合气体的试管倒立在水槽中,充分反应后,试管内残留气体10mL,则原混合气体中N2和NO2的体积之比是
[? ]
A.3∶1
B.1∶3
C.1∶2
D.2∶1
参考答案:B
本题解析:
本题难度:一般
3、计算题 Fe是人?体不可缺少的微量元素,摄入含铁化合物可补充铁。
(1)正常人每天应补充14?mg左右的铁。其?中绝大部分来自于食物。如果全部通过服用含FeSO4・7H2O的片剂来补充铁,则正常人每天服需用含________mg?FeSO4・7H2O的片剂。
(2)“速力菲”是市场上一种常见的补铁药物,其中Fe2+的含量为35.0%。该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率超过10%即不能再服用。为检验某药店出售的“速力菲”是否失效,取10.00?g该药品全部溶于稀硫酸,配制成1?000?mL溶液。取其中20.00?mL,用0.010?00?mol/L?KMnO4溶液滴定,用去KMnO4溶液24.00?mL。通过计算说明该药物是否能服用?(MnO4-在酸性条件下的还原产物为Mn2+,药品中除铁元素外其他成分不与KMnO4反应)
参考答案:(1)69.5
(2)5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O
n(Fe)=0.010?00?mol/L×24.00×10-3L×5×50=0.06?mol
m(Fe?)=0.06?mol×56?g/mol=3.36?g,
氧化率小于10%,所以可以服用。
本题解析:
本题难度:一般
4、选择题 向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入c mol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到同体pg。则下列关系不正确的是
[? ]
A. 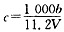
B. 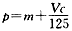
C. n=m+17Vc
D. 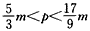
参考答案:C
本题解析:
本题难度:一般
5、计算题 将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为
11.2L。请回答:
(1)NO的体积为 L,NO2的体积为_______________ L。
(2)待产生的气体全部释放后,向溶液加入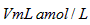 的NaOH溶液,恰好使溶液中的全部转化成沉淀,则原硝酸溶液的浓度为_______________ mol/L。 的NaOH溶液,恰好使溶液中的全部转化成沉淀,则原硝酸溶液的浓度为_______________ mol/L。
(3)欲使铜与硝酸反应生成的气体在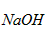 溶液中全部转化为 溶液中全部转化为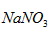 ,至少需要30%的双氧水____g。 ,至少需要30%的双氧水____g。
参考答案:(1)5.8 5.4
(2)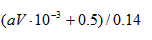
(3)57.8
本题解析:
本题难度:一般
|