微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列化学用语或模型表示正确的是
A.H2O2分子结构式:H一O一O一H
B.氮气的电子式:N 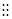 N
N
C.Mg2+结构示意图:
D.C2 H4分子比例模型: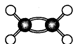
参考答案:A
本题解析:氮气的电子式为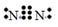 ,B项错误;Mg2+结构示意图
,B项错误;Mg2+结构示意图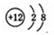 ,C项错误,D项为乙烯的球棍模型,不是比例模型。答案选A。
,C项错误,D项为乙烯的球棍模型,不是比例模型。答案选A。
点评:从近几年的考试题中可以看出,这类题主要考察的是原子(离子)的结构示意图,有机物的球滚模型或者比例模型,有机物的结构式或结构简式,原子、离子、化合物或取代基的电子式。要熟练掌握这些化学术语才能准确的回答这类问题。
本题难度:一般
2、填空题 写出化学反应方程式
(1)苯酚钠溶液中通入CO2______
(2)溴乙烷和氢氧化钠溶液共热______
(3)乙酸与乙醇发生酯化反应______.
参考答案:(1)苯酚钠通入二氧化碳生成苯酚和碳酸氢钠;反应的化学方程式为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3;故答案为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3;
(2)溴乙烷和氢氧化钠共热生成乙醇和溴化钠;反应的化学方程式为:CH3CH2Br+NaOH加热
本题解析:
本题难度:一般
3、选择题 下列所给粒子间的数量满足2:1关系的是
A.氧化钠中的氧离子和钠离子
B.二氧化硅中的硅原子和氧原子
C.过氧化钠中的钠离子和过氧根离子
D.碳酸溶液中的氢离子和碳酸根离子
参考答案:C
本题解析:A、氧化钠中氧离子和钠离子个数比1:2,错误;B、二氧化硅中的硅原子和氧原子1:2,错误;C、过氧化钠中的钠离子和过氧根离子2:1,正确;D、碳酸溶液部分电离,一级电离生成氢离子和碳酸氢根,二级电离生成氢离子和碳酸根离子,无法计算氢离子和碳酸根离子的比值,错误。
本题难度:一般
4、选择题 如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是(? )
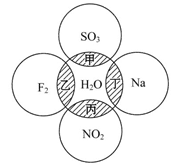
A.甲
B.乙
C.丙
D.丁
参考答案:C
本题解析:SO3与H2O的反应不是氧化还原反应;Na与H2O的反应是氧化还原反应,H2O是氧化剂;NO2与H2O的反应是氧化还原反应,H2O既不作氧化剂也不作还原剂;F2与H2O的反应是氧化还原反应,H2O是还原剂
本题难度:一般
5、选择题 中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是
A.Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同
B.SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强
C.H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO
D.根据常温下铜与浓硝酸可以制取NO2,推出常温下铁与浓硝酸也可以制取NO2
参考答案:C
本题解析:A.Na2O、Na2O2组成元素相同,但是与水发生的反应不同,Na2O+ H2O=2NaOH;2Na2O2+ 2H2O="4NaOH+" O2↑。产物也不同。错误。B.SO2和湿润的Cl2都有漂白性,若将二者按照一定比例混合后,则会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl。产生的H2SO4和HCl都没有漂白性。错误。C.根据复分解反应的规律:强酸制取弱酸。由于H2CO3的酸性比HClO强,所以将CO2通入NaClO溶液中能生成HClO。正确。D.在常温下铜与浓硝酸可以制取NO2,但是由于Fe的活动性比Cu强,在常温下铁遇浓硝酸会发生钝化现象。错误。
本题难度:一般