微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 (浙江省宁波市鄞州高级中学08-09学年高三上学期期中考试,化学,21)为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A.HCHO溶液(石蕊试液)
B.Na2SO3溶液(BaCl2)
C.KI(淀粉溶液)
D.FeCl2溶液(KSCN)
参考答案:B
本题解析:A项加入石蕊试液若变红,则HCHO溶液变质成HCOOH; B项中缺少稀盐酸,不能达到目的;C项加入淀粉溶液若变蓝,则KI氧化变质成I2;D项加入KSCN溶液后,若溶液变血红色,则FeCl2溶液氧化变质FeCl3溶液。
本题难度:简单
2、选择题 下列说法正确的是
A.某溶液中滴入AgNO3溶液,生成白色沉淀,该溶液中可能含Cl-
B.实验已经证明,氯水是可以导电的,所以氯水是电解质
C.某溶液与淀粉碘化钾溶液反应后出现蓝色,则证明该溶液是氯水
D.氟气跟氯化钠水溶液反应,有HF和O2生成
参考答案:AD
本题解析:A:正确
B:氯水是混合物,不可能属于电解质
C:只要能将I―氧化为碘,则就可出现蓝色现象,例如铁盐、硝酸溶液等
D:氟气与水发生了置换反应:2F2+2H2O=4HF+O2,正确
答案为AD
本题难度:一般
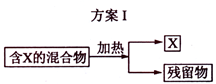
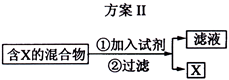
3、填空题 下图表示从固体混合物中分离X的2种方案,请回答有关问题。

 ?
?
 (1)选用方案I时,X应该具有的性质是?,残留物应该具有的性质是?;
(1)选用方案I时,X应该具有的性质是?,残留物应该具有的性质是?;
 (2)选用方案Ⅱ从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是?,有关反应的化学方程式为?;
(2)选用方案Ⅱ从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是?,有关反应的化学方程式为?;
 (3)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),参照方案I和Ⅱ,请设计一种以框图形式表示的实验方案(注明物质和操作)?。
(3)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),参照方案I和Ⅱ,请设计一种以框图形式表示的实验方案(注明物质和操作)?。
参考答案:1)加热时可升华,或易挥发?热稳定性好,且没有挥发性
(2)浓硝酸,Ag+2HNO3(浓) = AgNO3 ?+ NO2↑+ H2O;
Cu + 4 HNO3(浓) = Cu(NO3)2 + 2NO2↑+2 H2O
(3)

本题解析:(1)从题中给的信息可理解为升华或蒸馏,因此X的性质为加热时可升华,或易挥发。残留物必须热稳定性好,且没有挥发性。
(2)金、银、铜三种金属金的活泼性最差,不能与硝酸反应,选用硝酸作为试剂,过滤即可。
(3)三种氧化物中,SiO2、Al2O3都能与强碱发生反应,但Fe2O3不会反应,可以选浓NaOH溶液反应后过滤。但如果SiO2的含量大,则不宜用前面所述方法,可选用盐酸溶解,过滤后去除SiO2,再在混合液中加入过量的溶液,过滤得Fe(OH)3沉淀,洗涤后加热分解的方法。
本题难度:简单
4、选择题 下列各项操作错误的是
[? ]
A.用酒精萃取溴水中的溴单质可选用分液漏斗,而后静置分液
B.进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出
C.萃取、分液前需对分液漏斗检漏
D.为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下(或使塞子上的凹槽对准漏斗上的小孔)
参考答案:A
本题解析:
本题难度:简单
5、选择题 下列各组物质中,所含分子数目相同的是
A.10gH2和10gO2
B.9gH2O和0.5molBr2
C.224mLH2(标准状况)和0.1molN2
D.5.6LN2和11gCO2
参考答案:B
本题解析:分析:A.根据n=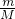 计算氢气、氧气的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
计算氢气、氧气的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
B.根据n=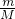 计算水的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
计算水的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
C.根据n=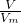 计算氢气物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
计算氢气物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
D.未指明氮气所处的状态,气体摩尔体积不一定是22.4L/mol.
解答:A.10gH2的物质的量=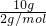 =5mol,10gO2的物质的量=
=5mol,10gO2的物质的量=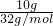 =
=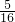 mol,二者物质的量不相等,含有的分子数目不相等,故A错误;
mol,二者物质的量不相等,含有的分子数目不相等,故A错误;
B.9gH2O的物质的量=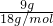 =0.5mol,与0.5molBr2的物质的量相等,含有的分子数目相等,故B正确;
=0.5mol,与0.5molBr2的物质的量相等,含有的分子数目相等,故B正确;
C.224mLH2(标准状况)的物质的量=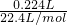 =0.01mol,与0.1molN2的物质的量不相等,二者含有的分子数目不相等,故C错误;
=0.01mol,与0.1molN2的物质的量不相等,二者含有的分子数目不相等,故C错误;
D.未指明氮气所处的状态,气体摩尔体积不一定是22.4L/mol,物质的量不一定是0.5mol,二者物质的量不一定相等,根据N=nNA可知,二者含有分子数目不一定相等,故D错误;
故选B.
点评:本题考查常用化学计量的有关计算,难度不大,注意对公式的理解与灵活运用,注意气体摩尔体积的使用条件与对象.
本题难度:一般