��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��6�֣���1��������ѹ50��������£���ƿ����ֱ���һ����̼�Ͷ�����̼����֪���ǵ�������ȣ���������������ԭ�ӵĸ���֮����_________,��ƿ������ܶ�֮����________.?
��2����ͬ��ͬѹ�£�2gCO2�����Ϊ1120mL����2gB��������Ϊ770mL��������B��Ħ������Ϊ______________��?
�ο��𰸣���6�֣� 11��14? 7��11? 64 g/mol ��ÿ��2�֣�
�����������1����������ȵ�����С��CO��CO2�����ʵ���֮����44�U28��11�U7��������ԭ����֮����11�U14���ܶ�֮������Է�������֮�ȣ�������7�U11��
��2������ͬ�����£���������֮������Ӧ�����ʵ���֮�ȣ�������2/44�U2/M��1120�U770�����M��64������B�����Ħ��������64g/mol��
�����Ѷȣ�һ��
2��ѡ���� ������Һ�е�������Ũ��Ϊ0.3mol�ML���ǣ�?��
A��150 ml0.1 mol��L NaCl��Һ
B��75 ml0.2 mol��L NH4Cl��Һ
C��300 ml0.1 mol��L K Cl��Һ
Cl��Һ
D��150 ml0.1 mol��L FeCl3��Һ
�ο��𰸣�D
�����������
�����Ѷȣ���
3��ѡ���� ������Һ�����ʵ����ʵ���Ũ��Ϊ1mol/L���ǣ�������
A��10gNaOH�����ܽ���ˮ�����250mL��Һ
B����22.4L�Ȼ�����������ˮ���1L��Һ
C����1L10mol/L��Ũ������9Lˮ���
D����58.5gNaCl��������1Lˮ��
�ο��𰸣�A��10gNaOH�����ʵ���Ϊ0.25mol������ˮ���0.25L��Һ������Ũ��Ϊ0.25mol0.25L=1mol?L-1����A��ȷ��
B��HCl������״̬��ȷ����22.4L HCl��һ����1mol������ˮ���1L��Һ����Ũ�Ȳ�һ����22.4L����B����
C����1L10mol/L��Ũ������9Lˮ��ϣ�������Һ���������10L��ϡ�ͺ��Ũ�Ȳ���1mol/L����C����
D��58.5gNaCl�����ʵ���Ϊ1mol������ˮ���1L��Һ������Ũ��Ϊ1mol/L�������ܼ������Ϊ1L����D����
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� һ������14%��KOH��Һ��������������100gˮ������������Ϊ28%�����Ϊ125mL����Ũ�����KOH�����ʵ���Ũ��Ϊ��������
A��2.2mol/L
B��4mol/L
C��5mol/L
D��6.25mol/L
�ο��𰸣���ԭKOH��Һ������Ϊx����
x��14%=��x-100����28%��
���x=200g��
KOH������Ϊ200g��14%=28g��
��n=28g56g/mol=0.5mol��
����Ũ�����KOH�����ʵ���Ũ��Ϊ0.5mol0.125L=4mol/L��
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� ��NAΪ�����ӵ�������ֵ������������ȷ����
A����״���£�22.4L��������춡��Ļ�������������õ��Ӷ���Ϊ14NA
B�����³�ѹ�£�15.0g��ȩ�������ǵĻ�����к�����ԭ�ӵ���ĿΪNA
C��60g SiO2��������Si��O������ĿΪ2NA ��78 g������C=C˫������ĿΪ3NA
D����CO2ͨ��Na2O2ʹ������a gʱ����Ӧ��ת�Ƶ�����Ϊ
�ο��𰸣�B
���������A���У���״���£�22.4L������1mol��������(CH3CH2CH2CH3)���춡��[(CH3)CHCH3]�����������õ��Ӷ�����Ϊ13����A����B���У���ȩ�������ǵ�ʵ��ʽ����CH2O����15.0g��ȩ�������ǵĻ�����к�����ԭ�ӵ���ĿΪNA˵����ȷ��C���У�SiO2����ƽ��1��Si��4��Si��O��������60g SiO2��������Si��O������ĿΪ4NA ���������в���>C=C<˫�����ʲ���ȷ��D���У���CO2ͨ��Na2O2ʹ������a g(������CO��28)����Ӧ��ת�Ƶ����� (1Na2O2ת��1e-)Ϊ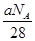 ����˵������AΪ�����ӵ�������ֵ����ʾ����Ŀ��
����˵������AΪ�����ӵ�������ֵ����ʾ����Ŀ��
�����Ѷȣ�һ��