��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ�У���ȷ���ǣ�?��
A����������������������Һ��Ӧ�� SO2+OH��=SO32��+H2O
B������������������Һ��Ӧ�� H++OH��=H2O
C������������ˮ��Ӧ�� 3NO2+H2O=NO+2H++2NO3��
D��������������������Һ��Ӧ�� Al2O3+2OH��=2AlO2��+H2
�ο��𰸣�C
���������A����������������������Һ��Ӧ�� SO2+OH-=SO32-+H2O��ԭ�Ӻ͵�ɲ��غ㣬����B������������������Һ��Ӧ�� H++OH-=H2O��©��SO42-��Ba2+�ķ�Ӧ������C������������ˮ��Ӧ�� 3NO2+H2O=NO+2H++2NO3-����ȷ��D��������������������Һ��Ӧ�� Al2O3+2OH-=2AlO2-+H2����Ӧ�����������
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����
A������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba(OH)2��Һ��ϣ�
2HCO3�� + Ba2++ 2OH��====BaCO3�� + CO32�� + 2H2O
B������ˮ�ⷴӦ��CO32�� + 2H2O H2CO3+ 2OH��
H2CO3+ 2OH��
C����ϡ��ˮ�м���ϡ���NH3��H2O + H+="===" NH4++ H2O
D��̼������ڴ����У�CaCO3 + 2H+ ="===" Ca2+ + H2O + CO2��
�ο��𰸣�C
���������
��ȷ�𰸣�C
A��ӦΪ: HCO3�� + Ba2+?+ OH��====BaCO3��? + H2O
B��ӦΪ��CO32�� + H2O HCO3 -+ OH��
HCO3 -+ OH��
D��ӦΪ��CaCO3 + 2CH3COOH="===" Ca2+ + H2O + CO2����2CH3COO�D
�����Ѷȣ���
3��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A���Ȼ�����Һ�м������ۣ�Fe+Fe3+=2Fe2+
B��Ư����Һ��ͨ�����������̼��Ca2++2ClO-+H2O+CO2=CaCO3��+2HClO
C��һС�������Ͷ��ˮ�У�2Na+2H2O=2Na++2OH-+H2��
D��С�մ���Һ���ռ���Һ��Ӧ��HCO3-+OH-=CO3-+H2O
�ο��𰸣�A�����ӷ���ʽ���ߵ�ɲ��غ㣬��ȷ�����ӷ���ʽΪ��Fe+2Fe3+=3Fe2+����A����
B��Ư����Һ��ͨ�����������̼��Ca��ClO��2+2CO2+2H20=Ca��HCO3��2+2HClO����ȷ�����ӷ���ʽΪ��ClO-+H20++CO2=HClO+HCO3-����B����
C��������Ϊ���ʣ�Ӧд�ɻ�ѧʽ��һС�������Ͷ��ˮ�У�2Na+2H2O=2Na++2OH-+H2������C��ȷ��
D��̼����������ӷ��Ŵ���С�մ���Һ���ռ���Һ��Ӧ����ȷ�����ӷ���ʽΪ��HCO3-+OH-=CO32-+H2O����D����
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� ����Cr�������ؽ���Ԫ�أ������ķ�ˮ�ͷ����ŷű��뾭�������ﵽ�йصİ�ȫ����
��1����ԭ�Ӻ���������Ϊ24����λ�����ڱ��е�______���ڡ�
��2����Ԫ����Cr2O72-����ʽ���������Է�ˮ�У�����FeSO4���仹ԭΪCr3�������ó��������з��롣��֪��

��FeSO4��ԭCr2O72-�����ӷ���ʽΪ______________________________________________��
��Cr2��SO4��3��Һ�м������NaOHŨ��Һ����Ӧ�����ӷ���ʽΪ_____________________��
�۳����������ˮ�е�Cr3����pHӦ���Ƶķ�Χ��________��
�����й��ڸ����仯�����˵������ȷ����________��
A��K2Cr2O7��һ�ֳ��õ�ǿ������
B������K2Cr2O7��Һ�����ڼ���˾���Ƿ�ƺ�ݳ�
C��������Ӳ�ȴ���ʴ���dz��õĶƲ����
�ο��𰸣���1����
��2����Cr2O72-��6Fe2����14H��=2Cr3����6Fe3����7H2O
��Cr3����4OH��=CrO2-��2H2O
��8��10����ABC
�����������1����Ϊ24��Ԫ�أ�λ��Ԫ�����ڱ��ĵ������ڡ�
��2����Fe2��������ΪFe3����Cr2O72-����ԭΪCr3����ע�ⷴӦ�������������½��еģ�
�ڸ�����֪��Ӧ��
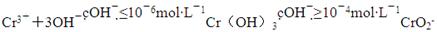
��֪��Cr3�������NaOH��Ӧ����ΪCrO2-��
�۸����ṩ��c��OH������֪Ӧ����pH�ķ�ΧΪ8��10��
��K2Cr2O7��Cr�Ļ��ϼ�Ϊ��ۣ���6�ۣ�������������ǿ������K2Cr2O7�������ƾ���������ɫ�仯��
�����Ѷȣ�һ��
5������� ��10�֣�д�����з�Ӧ�����ӷ���ʽ
(1) ��ϡ�����������(Fe2O3)??
(2) �ڳ���ʯ��ˮ�еμ�̼������Һ?
(3) FeCl3��Һ�м���NaOH��Һ��? ?
?
(4) ����ϡ���ᷴӦ��?
(5) ����CO2ͨ�����ʯ��ˮ�У�?
�ο��𰸣�
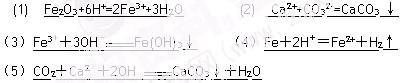
�����������
�����Ѷȣ�һ��