微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (10分)实验室有CuO和铜粉的混合物。要测定该样品(已称得其质量为m g)中氧化铜的质量分数。用下图所示仪器装置制取H2,再用H2还原CuO,最后根据样品质量的减少和无水CaCl2质量的增加来测定样品中氧化铜的质量分数。
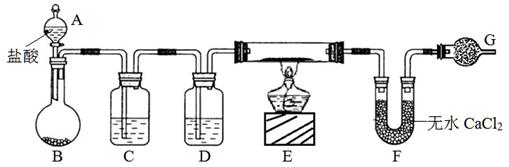
请回答:
(1)仪器中装入的试剂:D?。
(2)操作“①打开A的活塞”和“②点燃E处酒精灯”应该先进行的是?(填序号),在这两步操作之间还应进行的操作是:?。
(3)若实验中有部分CuO被还原为红色的Cu2O,对实验的影响为_____(偏大、偏小、无影响)。
(4)若测得的原质量为a g的硬质玻璃管(E),反应后质量变为b g;U型管实验后质量增加n g,由以上数据可以列出计算氧化铜质量分数的两个不同计算式:
计算式1:?;计算式2:?。
参考答案:(1)浓硫酸(1分)
(2)①(1分)收集G处的气体检验纯度(2分)
(3)偏小(2分)
(4)5(a-b)/m(2分) 40n/9m(2分)
本题解析:(1)由于生成的氢气中含有水蒸气,会干扰后面的实验,所以D中的盛放的应该是浓硫酸,用来除去水蒸气。
(2)由于装置中含有空气,所以应该首先生成氢气,将装置中的空气排尽。氢气是可燃性气体,再点燃之前,需要收集G处的气体检验纯度。
(3)若实验中有部分CuO被还原为红色的Cu2O,则生成的水就减少,因此氧化铜的质量分数就减少。
(4)根据方程式H2+CuO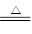 Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是
Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是 ,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是
,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是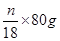 ,所以氧化铜的质量分数是40n/9m。
,所以氧化铜的质量分数是40n/9m。
本题难度:一般
2、实验题 (15分)浙江省“五水共治”是水质治理的重要举措,其中化学需氧量(COD)是水质测定中的重要指标,可以反映水中有机物等还原剂的污染程度。COD是指在一定条件下,用强氧化剂氧化水样中的还原剂及有机物时所消耗氧化剂的量,然后折算成氧化水样中的这些还原剂及有机物时需要氧气的量。某学习小组用重铬酸钾法测定某水样中的COD。主要的实验装置、仪器及具体操作步骤如下:
实验装置及仪器:

操作步骤:
①用仪器c将20.00mL水样置于250mL锥形瓶中,加入数粒碎瓷片。
②在水样中加入重铬酸钾标准溶液10.00mL,安装回流装置(如上图所示),从冷凝管上口加入30.00mL的H2SO4―Ag2SO4溶液,混匀后加热回流2h,充分反应。
③冷却后加指示剂2d,用硫酸亚铁铵溶液滴定多余重铬酸钾,至溶液由绿色变成红褐色。
已知:Cr2O72―+14H++6Fe2+=6Fe3++2Cr3++7H2O
请你回答下列问题:
(1)仪器c的名称:?;用仪器c吸取液体时,左手拿洗耳球,右手将仪器c插入溶液中吸取,当?时,立即用食指将管口堵住,将管尖离开液面,稍松食指使液面平稳下降,至凹液面最低处与标线相切,立即按紧管口。
(2)下列有关操作不正确的是?(用相应编号填写)
A.用硫酸亚铁铵溶液滴定时需上述仪器中的仪器b
B. 仪器c在使用时需要先用待取液进行润洗,管尖残留的液体一般不要吹出
C.加入数粒碎瓷片的作用是可以防止液体暴沸
D.上述操作步骤③中在滴定时判断滴定终点的指示剂可以是甲基橙
E.加热回流结束后,要用蒸馏水对冷凝管管壁进行冲洗
(3)在加热回流过程中,可以用水浴作为恒温加热源吗?同时请说明理由。?
(4)下列因素对测定水样中的COD能产生影响的有?(用相应编号填写)
①硫酸的用量? ②反应装置中的锥形瓶在反应前用蒸馏水洗涤?
③重铬酸钾的用量? ④回流时间的长短
(5)实验室配制重铬酸钾标准溶液的主要步骤及装置如下所示:
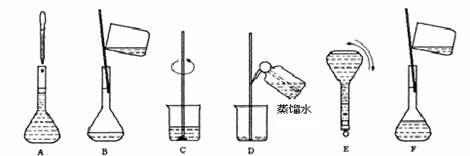
将上述实验步骤A到F按实验过程先后次序排列?
(6)已知:重铬酸钾标准溶液的c(Cr2O72―)=0.0250mol・L―1,硫酸亚铁铵溶液的c(Fe2+)=0.0100 mol・L―1,滴定终点时所消耗的硫酸亚铁铵溶液的体积为12.00mL,则按上述实验方法,测得的该水样的化学需氧量CODCr(O2)=?mg/L
参考答案:(1)移液管(2分)?溶液吸至标线以上(2分)?
(2)AD?(2分)?(3)不能,水浴温度不超过100。C ,难以使水样回流 (2分)
(4) ①③④?(2分)?(5) CBDFAE(2分)?(6)552?(3分)
本题解析:(1)根据仪器c的构造知,仪器c的名称为:移液管;用仪器c吸取液体时,左手拿洗耳球,右手将仪器c插入溶液中吸取,当溶液吸至标线以上时,立即用食指将管口堵住,将管尖离开液面,稍松食指使液面平稳下降,至凹液面最低处与标线相切,立即按紧管口。(2) A、硫酸亚铁铵溶液水解呈酸性,用硫酸亚铁铵溶液滴定时需上述仪器中的仪器a酸式滴定管,错误;B、移液管在使用时需要先用待取液进行润洗,管尖残留的液体一般不要吹出,正确; C、甲基橙的变色范围是3.1――4.4,铁离子转化为沉淀,不能用甲基橙作指示剂,错误; E、加热回流结束后,为使样品全部反应,要用蒸馏水对冷凝管管壁进行冲洗,正确;选AD;(3)在加热回流过程中,不能用水浴作为恒温加热源,理由是水浴温度不超过100。C ,难以使水样回流。(4)根据题给反应和信息知,①硫酸的用量③重铬酸钾的用量④回流时间的长短对测定结果有影响,选①③④;(5)实验室配制重铬酸钾标准溶液的主要步骤是计算、称量、溶解、转移、洗涤、定容、摇匀,结合题给装置知,实验步骤A到F按实验过程先后次序排列CBDFAE;(6)根据反应Cr2O72―+14H++6Fe2+=6Fe3++2Cr3++7H2O知,与硫酸亚铁铵溶液反应的重铬酸根的物质的量n=c(Fe2+)V(Fe2+)/6=0.0100 mol・L―1×0.012L÷6=2×10―5mol,则与20mL水样反应的重铬酸根的物质的量n=2.5×10―4mol ―2×10―5mol =2.3×10―4mol,根据电子守恒知,转化成氧气的物质的量为3.45×10―4mol,则按上述实验方法,测得的该水样的化学需氧量CODCr(O2)=552mg/L。
本题难度:一般
3、实验题 某同学利用下面装置实现铜与浓、稀硝酸的反应,过程如下:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ.按下图所示连接仪器,检查气密性,装入化学试剂。

(1)过程I发生反应的离子方程式是____________________。
(2)过程Ⅱ将铜丝做成螺旋状的目的是________________。
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是___________。当红棕色气体较多时,轻抽注射 器使反应停止,关闭a,取下注射器。生成红棕色气体的化学反应方程式是____________________。
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体产生。稀硝酸充满玻璃管的实验目的是___________。
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示:

①根据上表得出的结论是_______________。
②查阅资料:
a.NO2与水反应的实际过程为2NO2+H2O=HNO3+HNO2、3HNO2=HNO3+2NO↑+H2O
b.HNO2不稳定。
产生上述现象的原因是_______________________。
参考答案:(1)Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O
(2)增大铜丝与酸的接触面积,提高化学反应速率
(3)①打开止水夹a和b,用注射器向装置中推入空气;Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;②将玻璃管中的NO2排出
(4)①温度越低,进入试管中的溶液越多;②温度降低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管中的溶液多
本题解析:
本题难度:一般
4、实验题 (15分)某小组以CoCl2・6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1mLc1 mol・L―1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol・L―1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
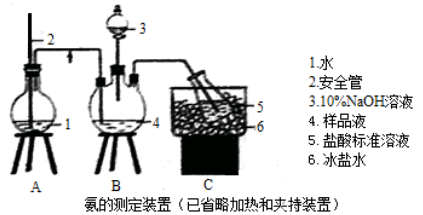
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是?。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用?式滴定管,可使用的指示剂为?。
(3)样品中氨的质量分数表达式为?。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将?(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是?;滴定终点时,若溶液中c(Ag+)=2.0×10―5 mol・L―1,c(CrO42―)为?mol・L―1。(已知:Ksp(Ag2CrO4)=1.12×10―12)
(6)经测定,样品X中钴.氨.氯的物质的量之比为1:6:3,钴的化合价为?,制备X的化学方程式为?;X的制备过程中温度不能过高的原因是?。
参考答案:
当A中压力过大时,安全管中液面上升,使A瓶中压力稳定
碱?酚酞(或甲基红)
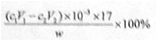
偏低
防止硝酸银见光分解? 2.8×10―3
+3? 2CoCl2+2NH4Cl+10NH3+H2O2 2[Co(NH3)6]Cl3+2H2O?温度过高过氧化氢分解、氨气逸出
2[Co(NH3)6]Cl3+2H2O?温度过高过氧化氢分解、氨气逸出
本题解析:(1)分析题给装置知,装置中安全管的作用原理是当A中压力过大时,安全管中液面上升,使A瓶中压力稳定。(2)用NaOH标准溶液滴定过剩的HCl时,应使用碱式滴定管,可使用的指示剂为酚酞(或甲基红)。(3)根据题给信息知,氨的测定过程中发生反应HCl+NH3 NH4Cl,则样品中氨的物质的量与和氨气反应的HCl的物质的量相等,为(c1V1―c2V2)×10―3mol,则氨气的质量为
NH4Cl,则样品中氨的物质的量与和氨气反应的HCl的物质的量相等,为(c1V1―c2V2)×10―3mol,则氨气的质量为
(c1V1―c2V2)×10―3×17g,质量分数表达式为 。(4)测定氨前应该对装置进行气密性检验,若气密性不好会导致氨气逸出,测定结果将偏低。(5)测定氯的过程中,用硝酸银溶液滴定,硝酸银见光易分解,故使用棕色滴定管的原因是防止硝酸银见光分解;根据沉淀溶解平衡知识知,c(CrO42―) =Ksp(Ag2CrO4)/ c2(Ag+)= 1.12×10―12/(2.0×10―5)2=2.8×10―3mol・L―1。(6)根据题意知,样品X中钴、氨、氯的物质的量之比为1:6:3,则X的化学式为[Co(NH3)6]Cl3,利用化合价规则判断,钴的化合价为+3;根据题给信息知,CoCl2・6H2O、NH4Cl、H2O2、浓氨水在活性炭催化下,合成橙黄色晶体X,化学方程式为2CoCl2+2NH4Cl+10NH3+H2O2
。(4)测定氨前应该对装置进行气密性检验,若气密性不好会导致氨气逸出,测定结果将偏低。(5)测定氯的过程中,用硝酸银溶液滴定,硝酸银见光易分解,故使用棕色滴定管的原因是防止硝酸银见光分解;根据沉淀溶解平衡知识知,c(CrO42―) =Ksp(Ag2CrO4)/ c2(Ag+)= 1.12×10―12/(2.0×10―5)2=2.8×10―3mol・L―1。(6)根据题意知,样品X中钴、氨、氯的物质的量之比为1:6:3,则X的化学式为[Co(NH3)6]Cl3,利用化合价规则判断,钴的化合价为+3;根据题给信息知,CoCl2・6H2O、NH4Cl、H2O2、浓氨水在活性炭催化下,合成橙黄色晶体X,化学方程式为2CoCl2+2NH4Cl+10NH3+H2O2 2[Co(NH3)6]Cl3+2H2O;X的制备过程中温度不能过高的原因是温度过高过氧化氢分解、氨气逸出。
2[Co(NH3)6]Cl3+2H2O;X的制备过程中温度不能过高的原因是温度过高过氧化氢分解、氨气逸出。
本题难度:一般
5、实验题 某班同学用如图所示的装置测定空气里氧气的含量。药匙上放少量钠,烧杯中装满水,先用弹簧夹夹住橡胶管。点燃钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。
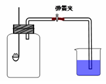
(1)写出燃烧匙中发生反应的化学方程式:?,将该生成物伸入瓶底的水中,生成的氧化产物与还原产物物质的量之比为:?。
(2)实验完毕,广口瓶内水面上升明显小于空气体积的1/5,对这一现象解释正确的是:?
a.该同学可能未塞紧瓶塞,导致钠熄灭时外界空气进入瓶内
b.该同学可能使用钠的量不足
c.该同学可能没夹紧弹簧夹,钠燃烧时部分空气受热从导管逸出
d.该同学可能插入燃烧匙太慢,塞紧瓶塞前瓶内部分空气受热逸出
参考答案:(1)2Na+O2 Na2O2;1:2?(2)ab
Na2O2;1:2?(2)ab
本题解析:该实验利用金属钠燃烧消耗集气瓶集气瓶内氧气,压强减小,回复室温后,打开弹簧夹,烧杯内的水进入集气瓶,水的体积就是消耗掉氧气的体积。金属钠燃烧反应生成Na2O2,2Na2O2+2H2O=4NaOH+O2,Na2O2既是氧化剂又是还原剂,氧化产物是氧气,NaOH有一半是还原产物,氧化产物与还原产物物质的量之比为1:2,最后水的体积小,说明所测结果体积偏小,a导致外界空气进入装置,倒流回去的水偏少,正确;b、钠不足,没有把氧气消耗完,所测体积少,正确;c、空气溢出,水倒流的应该更多,错误;d、空气溢出,水倒流的应该更多,错误。
本题难度:一般