微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关钢铁腐蚀说法正确的是( )
A.钢铁腐蚀时铁作正极
B.钢铁腐蚀时铁发生的反应为:Fe-3e?-=Fe3+
C.在碱性环境中正极反应式为:O2+2H2O+4e-=4OH-
D.在酸性环境中正极反应式为:O2+4H++4e-=2H2O
参考答案:A.无论析氢腐蚀还是吸氧腐蚀,铁都作负极,碳作正极,故A错误;
B.钢铁腐蚀时铁失电子生成亚铁离子,发生氧化反应,电极反应式为:Fe-2e?-=Fe2+,故B错误;
C.碱性环境中,钢铁发生吸氧腐蚀,正极上氧气得电子发生还原反应,所以电极反应式为:O2+2H2O+4e-=4OH-,故C正确;
D.酸性环境中,钢铁发生析氢腐蚀,正极上氢离子得电子生成氢气,电极反应式为:2H++2e-=H2↑,
故D错误;
故选C.
本题解析:
本题难度:一般
2、选择题 用如图所示装置进行实验,下列叙述不正确的是 (?)

A.K与N连接时,铁被腐蚀
B.K与N连接时,石墨电极产生气泡
C.K与M连接时,一段时间后溶液的pH增大
D.K与M连接时,石墨电极反应式:4OH--4e-=2H2O+O2↑
参考答案:D
本题解析:K与N连接时,构成原电池,发生析氢腐蚀,A、B正确;K与M连接时,电极反应式为阳极:2Cl--2e-=Cl2↑,阴极:2H++2e-=H2↑,D项错误。
本题难度:一般
3、填空题 (10分)钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
_________________________?。(2分)
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式______________________。(2分)
(3)下列哪些装置可防止铁棒被腐蚀_____________ 。(1分)
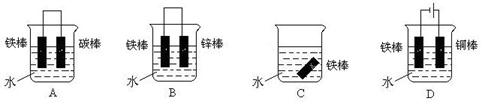
(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:
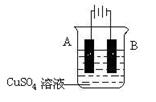
请回答:
① A电极对应的金属是?(写元素名称),(1分)B电极的电极反应式是?。(2分)
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:?。(2分)
参考答案:(1)Fe2O3 + 3CO  ?2Fe + 3CO2?(2)FeCl3 + Fe = 3FeCl2?(3)BD
?2Fe + 3CO2?(2)FeCl3 + Fe = 3FeCl2?(3)BD
(4)①铜(写元素名称),Cu2+ + 2e- = Cu
②铁比铜活泼,镀层铜被破坏后形成的原电池铁做负极,腐蚀加快,而镀锌刚好相反
本题解析:铁锈的主要成份为:Fe2O3 ・2H2O;
(2)加入盐酸:Fe2O3 +6HCl="2" FeCl3 +3H2O ;
当铁锈被除尽后,即可发生如下反应:2FeCl3+Fe = 3FeCl2
(3)金属的防腐一般可通过牺牲阳极法、电镀法、电解池作阴极法。
(4)电镀时镀件为阴极、镀层金属为阳极。
本题难度:简单
4、选择题 下列事实不能用电化学理论解释的是?(?)
A.轮船水线下船壳上装有一定数量的锌块
B.粗锌比纯锌制H2更快
C.镀锌铁比镀锡铁耐用
D.银质奖章长期放置后表面会变暗
参考答案:D
本题解析:A属于牺牲阳极的银镜保护法,粗锌中含有杂质,可以构成原电池加快反应速率。活泼性顺序是锌>铁>锡,即镀层破损后镀锌铁若发生腐蚀,锌是负极,保护铁。银质奖章长期放置后表面会变暗,属于银的化学腐蚀,而不是电化学腐蚀。答案是D。
本题难度:一般
5、选择题 下图各容器中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序是
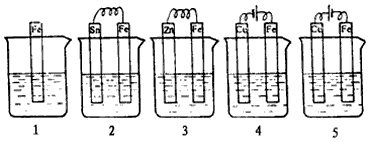
[? ]
A.4>2>1>3>5
B.2>1>5>3>4
C.5>2>1>3>4
D.4>3>1>2>5
参考答案:A
本题解析:
本题难度:简单