微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列分子中有3个原子核的是( )
A.HF
B.NH3
C.H2O
D.CH4
参考答案:C
本题解析:
本题难度:简单
2、简答题 回答下列问题:
(1)
S2-微粒中的中子数是______,核外电子数是______.若阿伏加德罗常数用NA表示,49.5g34SO2含有______个原子.S原子的结构示意图______.
(2)3.01×1023个HCl分子的物质的量是______mol,其在标准状况下的体积为______L,将其溶于水配成2L溶液,所得溶液的物质的量浓度为______mol/L.
(3)在工农业生产和日常生活中经常用到下列物质:①Si;②Ca(ClO)2;③Al(OH)3;④Fe2O3.其中,可用于制造芯片的是______(填序号,下同);可用于杀菌,消毒的是______;可用作红色油漆和涂料的是______;医疗上可用作胃酸中和剂的是______.
参考答案:(1)3416S2-微粒的质子数为16,质量数为34,中子数=34-16=18,核外电子数=16+2=18;
49.5g 34SO2的物质的量为49.5g66g/mol=0.75mol,1个34SO2中含有3个原子,所以有49.5g 34SO2含有2.25NA个原子;
硫原子的结构示意图为: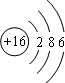 ;
;
故答案为:18;18;2.25NA; ;
;
(2)HCl分子的物质的量n(HCl)=NNA=3.01×10236.02×1023/mol=0.5mol,在标准状况下的体积其体积V(HCl)=0.5mol×22.4L/mol=11.2L,将其溶于水配成2L溶液,所得溶液的物质的量浓度为
c(HCl)=0.5mol2L=0.25mol/L,
故答案为:0.5;11.2;0.25;
(3)①Si原子最外层电子为4个,既难得电子,也难失去电子,可做为半导体,可用于制造硅芯片;
②Ca(ClO)2中+1价的氯具有强氧化性,能与还原性物质作用变成-1价的氯,可用于杀菌、消毒;
③Al(OH)3具有两性,作为酸时,酸性较弱,作为碱时,碱性较弱,胃酸的成分为盐酸,氢氧化铝显弱碱性,和盐酸发生中和反应,Al(OH)3医疗上可用作胃酸中和剂;
④Fe2O3是氧化物,颜色为红棕色,俗称为铁红,可用作红色油漆和涂料;
故答案为:①;②;④;③;
本题解析:
本题难度:一般
3、选择题 元素A、B、C原子核内质子数之和为31,最外层电子数之和为17,这三种元素是
[? ]
A、?N、P、Cl ?
B、?P、O、S ?
C、?N、O、S ?
D、?O、F、Cl
参考答案:C
本题解析:
本题难度:简单
4、选择题 科学家最近制造出第112号新元素,其原子的质量数为277,这是迄今已知元素中最重的原子.关于该新元素的下列叙述正确的是( )
A.其原子核内中子数和质子数都是112
B.其原子核内中子数为165,核外电子数为112
C.其原子质量是12C原子质量的277倍
D.其原子质量与12C原子质量之比为277:12
参考答案:A、因原子中原子序数=质子数=核电荷数=核外电子数,所以新元素的质子数为112,又因中子数=质量数-质子数=277-112=165,故A错误;
B、因原子中原子序数=质子数=核电荷数=核外电子数,所以核外电子数为112,又因中子数=质量数-质子数=277-112=165,故B正确;
C、因原子质量的质量之比=相对原子质量之比=原子的质量数之比,其原子质量与12C原子质量之比为277:12,故C错误;
D、因原子质量的质量之比=相对原子质量之比=原子的质量数之比,其原子质量与12C原子质量之比为277:12,故D正确;
故选:B、D.
本题解析:
本题难度:一般
5、选择题 下列说法中,正确的是
[? ]
A.?含金属元素的离子不一定是阳离子
B.?只有原子才满足核内质子数和核外电子数相等
C.?相同条件下,l?molH原子所具有的能量小于0.5?mol?H2所具有的能量
D.?蛋白质溶液、淀粉溶液和葡萄糖溶液都是胶体
参考答案:A
本题解析:
本题难度:简单