��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��NA���������ӵ���������ֵ������˵������ȷ����
�ٳ��³�ѹ�£�17 g������14CH3��������������Ϊ9NA
�ڳ��³�ѹ�£�22.4 L NO����ķ�����С��NA
��56 g����16g���ַ�Ӧ��ʧȥ2NA������
�ܳ��³�ѹ�£�100 mL 0.5 mol/L��������Һ�У�����ķ�����ĿС��0.05NA
�ݱ�״���£�22.4 L���ȼ��������еķ�����ΪNA
���³�ѹ�£�1 mol�������еĺ��������Ϊ4NA
��1mol/LNaCl��Һ��ʾ1Lˮ�к���NaCl 58.5g
��1molO2�����������Ʒ�Ӧ���õ���4mol e?
�ͬ���ʵ���Ũ������������Ϻ���Һ���ʵ���Ũ�ȱ�Ϊԭ���͵�һ��
��1 mol Na2O2�����к�������������ΪNA
A���٢ڢ�
B���ۢܢ�
C���ڢܢ�
D���ݢޢ�
�ο��𰸣�C
���������������14CH3������Է���������17��������������14��6��8�����Գ��³�ѹ�£�17g������14CH3��������������Ϊ8NA���ٲ���ȷ�����³�ѹ�£������Ħ���������22.4L/mol������22.4 L NO����ķ�����С��NA������ȷ��56g����16g������ʵ����ֱ���1mol��0.5mol�����߳�ַ�Ӧ����FeS����������S���㣬����ʧȥNA�����ӣ��۲���ȷ�����³�ѹ�£�100 mL 0.5 mol/L��������Һ�����ʵ����ʵ�����0.05mol������������������ʣ����ڵ���ƽ�⣬������Һ������ķ�����ĿС��0.05NA������ȷ����״���£����ȼ��鲻����̬����������������Ħ���������ˣ�22.4 L���ȼ�������ʵ�������1mol���ݲ���ȷ��He�ǵ�ԭ�ӷ��ӣ����³�ѹ�£�1 mol�������еĺ��������Ϊ2NA������ȷ��1mol/LNaCl��Һ��ʾ1L��Һ�к���NaCl 58.5g���߲���ȷ��1molO2�����������Ʒ�Ӧ������������������ƣ�Ҳ�����ǹ������ƣ����Բ���ȷ��ת�Ƶ��ӵ����ʵ��������ȷ��������ܶ�����ҺŨ�ȵ������������˲�ͬ���ʵ���Ũ������������Ϻ���Һ���ʵ���Ũ�Ȳ����ܱ�Ϊԭ���͵�һ�룬���ȷ���������ƾ������������ӵĸ���֮����1:2������1mol Na2O2�����к�������������ΪNA������ȷ����ѡC��
�����Ѷȣ�һ��
2��ѡ���� ������Һ�����ʵ���Ũ��Ϊ1mol/L����
A����40gNaOH �ܽ���1Lˮ��
B����22.4LHCl��������ˮ���1 L��Һ
C����1L 10 mol/L��Ũ�������9 Lˮ��
D����10 g NaOH�ܽ�������ˮ�У��ټ�����ˮֱ����Һ���Ϊ250 mL
�ο��𰸣�D
�������������c��n/V��֪��ѡ��A����ȷ����Һ���������1L��ѡ��B����ȷ����Ϊ��һ�����ڱ�״���£�ѡ��C�У���Һ���������10L�������ȷ�Ĵ�ѡD��
�����Ѷȣ�һ��
3��ѡ���� NA��ʾ�����ӵ�������ֵ������˵������ȷ���ǣ�?��
A��7��8 gNa2S��7��8 gNa2O2�к��е���������Ŀ��Ϊ0��1 NA
B��0��1mol��L-1��NaHSO4��Һ�к��������ӵ����ʵ���Ϊ0��2mol
C�����³�ѹ�£���ԭ������Ϊ0��2NA��SO2��O2�Ļ�����壬�����Ϊ2��24 L
D��l��8 g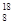 O2������1��8 g
O2������1��8 g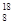 O3�����к��е�����������ͬ
O3�����к��е�����������ͬ
�ο��𰸣�A
���������Na2S��NaO2���������������ӵĸ���֮�ȶ���1�U2�ģ��Ҷ��ߵ�Ħ��������ȣ�����78g/mol������ѡ��A��ȷ��ѡ��B����ȷ����Ϊ����ȷ����Һ�������ѡ��C����ȷ����Ϊ�����״̬�����ڱ�״���£����������������Ԫ���γɵIJ�ͬ���ʣ���������ȵ������£���ԭ�ӵ����ʵ�������ȵģ�����ѡ��D�У�����������ȵģ���ѡA��
�����Ѷȣ�һ��
4��ѡ���� 2008��5���ҹ��봨���������ֺ���������������������Ա��Ϊ����0.01mol?L-1��KMnO4����Һ�����в�������������ҺŨ��ƫ����ǣ�������
A��δ����Һ��ȴ�����¾�ת�Ƶ�����ƿ��
B������ʱ�����ӿ̶���
C���ܽ����ʱ��Һ��ɽ�
D������ƿδ�������������ˮ
�ο��𰸣�A��δ����Һ��ȴ�����¾�ת�Ƶ�����ƿ�У�������Һ�����ƫС�������Ƶ���ҺŨ��ƫ��Aѡ��
B������ʱ���Ӷ�ȡ�̶ȣ���Һ��ʵ�����ƫ��cƫС����B��ѡ��
C���ܽ����ʱ��Һ��ɽ������ʵ�����ƫС��cƫС����C��ѡ��
D��ԭ����ƿϴ����δ�����ʵ������Ӱ�죬��D��ѡ��
��ѡA��
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪1.505��1023��X������ӵ�����Ϊ8g����X�����Ħ�������ǣ� ��
A��16g
B��32g
C��64g /mol
D��32g /mol