|
�߿���ѧ֪ʶ����ɡ�������ʵ���ƽ�⡷��Ƶ������ѵ��2017����ϰ�棩(��)
2017-09-23 22:47:23
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����£�����˵����ȷ����?
[? ]
A����pH=1��H2SO4��pH=3��HCl�������ϣ�������ҺpH=2
B��HF��HCN���룬��NaF��Һ��pH��ͬŨ��NaCN��Һ��pH��
C����0.1?mol/LCH3COOH��Һ�м�������CH3COONa���壬��Һ��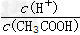 ���� ����
D����1?mL?pH��3��HX��Һϡ�͵�10?mL������Һ��pH��4����HXΪ����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
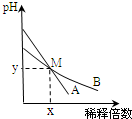
2��ѡ���� �����£�pH���1������һԪ����ҺA��B���ֱ��ˮϡ��ʱ����Һ��pH�仯��ͼ��ʾ������˵����ȷ���ǣ�������
A��ϡ��ǰ��c��A��=10?c��B��
B��ϡ��ǰ��A��Һ����ˮ�������OH-��Ũ�ȴ���10-7?mol/L
C����M�㣬A��B���ּ���Һ�������ӵ����ʵ���Ũ�����
D���ô����к�A��Һ��ǡ����ȫ��Ӧʱ����Һ��pHΪ7
| 
�ο��𰸣�A��ϡ��ǰ��c��AOH��=0.1mol/L��c��BOH����0.01mol/L����c��AOH����10c��BOH������A����
B��ϡ��ǰA��Һ������������Ũ�ȴ���B��Һ�У���������ˮ�ĵ��룻ϡ��ǰ��A��Һ����ˮ�������OH-��Ũ��С��10-7?mol/L����B����
C��M��AB��ҺpH��ͬ������������Ũ����ͬ������M��A��B���ּ���Һ�������ӵ����ʵ���Ũ����ȣ���C��ȷ��
D���ô����к�A��Һ��ǡ����ȫ��Ӧʱ�����������ᣬ���ɵĴ��������ˮ���Լ��ԣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ͬ�¶ȣ�Ũ�Ⱦ�Ϊ0.1mol /L���������������Һ����HF��Һ����CH3COOH��Һ����NaHCO3��Һ����֪���١��ڷֱ���ۻ�ϣ�ʵ���ò�����CO2���������v����ʱ�䣨t���ı仯����ͼ��ʾ������˵����ȷ���ǣ�? )
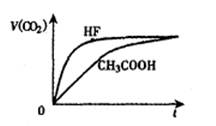
A������������Һ�У�c( OH��)��С���� > �� > ��
B���������ԵıȽϣ�CH3COOH > HF > H2CO3
C����Ӧ��������������Һ�У� c ( CH3COO�� ) > c ( F�� )
D���ٺ͢۷�Ӧ������������Һ�У�c ( F�� ) + c (HF) =" 0.10mol" /L
�ο��𰸣�A
���������A.������ͬŨ�ȵ�HF��NaHCO3��Ӧ�ų�CO2��CH3COOH��Һ�졣˵����Һ������HF> CH3COOH>H2CO3����Һ������Խǿ��c(H+)Խ�������ˮ�����ӻ������ɵ�c( OH��)��ԽС�����c( OH��)��С���� > �� > �١���ȷ��B. �������ԵıȽϣ�HF >CH3COOH > H2CO3������C. ��Ӧ���������ڷų���CO2�����ͬ�����Ժ��е�������ӵ�Ũ��Ҳ��ȡ�D. �ٺ͢۷�Ӧ������������Һ�У�c ( F�� ) + c (HF)? =" 0.05mol" /L .����
�����Ѷȣ�һ��
4��ѡ���� ���жԸ���ƽ����ϵ�������У���ȫ��ȷ��һ���ǣ�������
���к�10mL0.1mol/L�İ�ˮ���к�100mL0.01mol/L�İ�ˮ������ͬһŨ������������ͬ��
�ڳ����£���CH3COONa��Һ�м������������ᣬ��ʹ��ˮ��ƽ�������ƶ���
��ij�¶��£��ݻ�һ�����ܱ������н��п��淴Ӧ��X��g��+Y��g��?2Z��g��+W��g����H��0��ƽ��������¶ȣ�c��Z������
�ܸ��¼���MgCl2?6H2O����IJ���ΪMgCl2��H2O��
��һ��Ũ�ȵ�̼������Һ��ʹ��̪��Һ��죬��ԭ������Һ�д�������ƽ�⣺CO32-+H2O?HCO3-+OH-��ʹ����Һ�е�c��OH-����c��H+����
����̼��Ƶij����ܽ�ƽ����ϵ�У�ͨ��CO2���壬ƽ�����ܽ�ķ����ƶ���
�����Ȼ����ij����ܽ�ƽ����ϵ�У�����⻯�ع��壬�Ȼ���������ת��Ϊ�⻯��������
A���٢ڢۢܢ�
B���ڢۢܢݢ�
C���ڢۢݢޢ�
D���٢ڢݢޢ�
�ο��𰸣�����O��OL��0.1moL/L=0.1L��0.01moL/L�������ʵ����ʵ�����ͬ�����ĵ���������ʵ���Ҳ��ͬ���ʴ���
�ڴ�����ˮ�����ɴ��ᣬ��������ᣬ����Ũ��������ƽ���������ƶ�������ȷ��
������Ӧ���ȣ��¶����ߣ�ƽ��������Ӧ�����ƶ���c��Z��������ȷ��
�ܼ����Ȼ�þ��Һ���ٽ�þ���ӵ�ˮ�⣬���յõ�������þ���ʴ���
��̼����Ϊǿ�������Σ�ˮ��ʼ��ԣ���ʹ��̪��Һ��죬����ȷ��
��̼�����Һ��ͨ�������̼��������̼����ƣ�ƽ�����ܽ�ķ����ƶ�������ȷ��
�ߵ⻯�����ܶȻ�С���Ȼ����������Ȼ����ij����ܽ�ƽ����ϵ�У�����⻯�ع��壬�Ȼ���������ת��Ϊ�⻯������������ȷ��
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʱ������������ȷ���ǣ�������
A��ϡ��pH=10�İ�ˮ����Һ���������ӵ�Ũ�Ⱦ�����
B��pH��Ϊ5��HCl��NH4Cl��Һ�У�ˮ�ĵ���̶���ͬ
C��NaOH��CH3COONa�Ļ����Һ�У�c��Na+��+c��H+���Tc��OH-��+c��CH3COO-��
D���ֱ��к�pH���������ͬ������ʹ��ᣬ���������������Ƶ����ʵ�����
�ο��𰸣�A��ϡ�Ͱ�ˮ���ٽ�һˮ�ϰ����룬��Һ������������Ũ�ȼ�С��ˮ�����ӻ��������䣬��������Ũ������A����
B����������ˮ���룬�Ȼ�林ٽ�ˮ���룬����������Һ��ˮ�ĵ���̶Ȳ�ͬ����B����
C�����ݵ���غ��c��Na+��+c��H+���Tc��OH-��+c��CH3COO-������C��ȷ��
D���������pH�Ĵ�������ᣬ��������ʵ������������������ӵ����ʵ��������Էֱ��к�pH���������ͬ������ʹ��ᣬ���������������Ƶ����ʵ����࣬��D����
��ѡC��
���������
�����Ѷȣ�һ��
| 