微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在容积可变的密闭容器中,2mo1 N2和8mo1 H2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时的氮气的体积分数接近于( )
A.5%
B.10%
C.15%
D.20%
2、填空题 298 K时,合成氨反应:N2(g)+3H2(g) 2NH3(g),生成2 mol NH3放出92.4 kJ热量。在该温度下,取1 mol N2(g)和3 mol H2(g)在密闭容器中充分反应,放出的热量 (填“等于”“大于”或“小于”)92.4 kJ。原因是 _____________________________
2NH3(g),生成2 mol NH3放出92.4 kJ热量。在该温度下,取1 mol N2(g)和3 mol H2(g)在密闭容器中充分反应,放出的热量 (填“等于”“大于”或“小于”)92.4 kJ。原因是 _____________________________
3、填空题 一定条件下,体积为1 L的密闭容器中发生如下反应:SiF4(g)+2H2O(g) SiO2(s)+4HF(g) ΔH=+148.9 kJ・mol-1。
SiO2(s)+4HF(g) ΔH=+148.9 kJ・mol-1。
(1)下列各项中能说明该反应已达化学平衡状态的是________(填字母序号)。
a.v消耗(SiF4)=4v生成(HF)
b.容器内气体压强不再变化
c.容器内气体的总质量不再变化
d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示。
反应时间/min
| n(SiF4)/mol
| n(H2O)/mol
|
0
| 1.20
| 2.40
|
t1
| 0.80
| a
|
t2
| b
| 1.60
|
通过a或b的值及化学平衡原理说明t1时反应是否达到化学平衡状态:________。
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应________(填序号)。
a.一定向正反应方向移动
b.一定向逆反应方向移动
c.一定是减小压强造成的
d.一定是升高温度造成的
e.SiF4的平衡转化率一定增大
4、选择题 下列各图是温度T(或压强P)对f反应2A(s) + 2B(g) 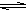 ?2C(g) + D(g)?△H>0的正、逆反应速率的影响,曲线交点表示建立平衡时的温度或压强,其中正确的是
?2C(g) + D(g)?△H>0的正、逆反应速率的影响,曲线交点表示建立平衡时的温度或压强,其中正确的是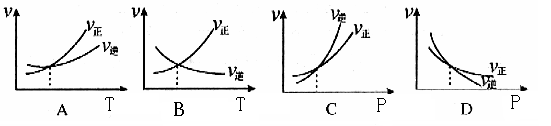
5、简答题 (14分)研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:①Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g)?△H 1 = +489.0 kJ・mol-1
?②C(石墨) +CO2(g) = 2CO(g)?△H 2 = +172.5 kJ・mol-1
则CO还原Fe2O3(s)的热化学方程式为?。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g)?△H
CH3OH(g) +H2O(g)?△H
①该反应的平衡常数表达式为K=???。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的ΔH?0 (填“>”、“<”或“=”)。

③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ?KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为?。
当氨碳比 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为:?。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为:?。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为?。