微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列解释事实的离子方程式正确的是
A.向铜片中滴加浓硫酸并加热,有刺激性气体产生:Cu+4H++SO42-Cu2++SO2↑+2H2O
B.向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++HCO3-+OH-═CaCO3↓+H2O
C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后变蓝:4H++4I-+O2═2I2+2H2O
D.服用阿司匹林过量出现水杨酸()反应,可静脉注滴NaHCO3溶液:+2HCO3-→+2CO2↑+2H2O
参考答案:C
本题解析:分析:A.浓硫酸在离子反应中保留化学式;
B.Ca(HCO3)2完全反应,反应生成碳酸钙、碳酸钠、水;
C.发生氧化还原反应生成碘和水;
D.只有-COOH能与碳酸氢钠反应.
解答:A.向铜片中滴加浓硫酸并加热,有刺激性气体产生的离子反应为Cu+2H2SO4(浓)  Cu2++SO42-+SO2↑+2H2O,故A错误;
Cu2++SO42-+SO2↑+2H2O,故A错误;
B.向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成的离子反应为Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B错误;
C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后变蓝的离子反应为4H++4I-+O2═2I2+2H2O,故C正确;
D.服用阿司匹林过量出现水杨酸( )反应,可静脉注滴NaHCO3溶液的离子反应为
)反应,可静脉注滴NaHCO3溶液的离子反应为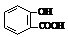 +HCO3-→
+HCO3-→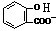 +CO2↑+H2O,故D错误;
+CO2↑+H2O,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,明确发生的化学反应是解答的关键,注意与量有关的离子反应为解答的难点,题目难度不大.
本题难度:困难
2、选择题 下列说法中正确的是?( )
A.s区都是主族元素
B.s区都是金属元素
C.稀有气体在ds区
D.所有非金属元素都在p区
参考答案:A
本题解析:试题分析:区的名称来自于按照构造原理最后填入电子的轨道名称,由此可知s区都是主族元素,A正确;氢元素在s区,属于非金属,B和D不正确;稀有气体在p区,C不正确,答案选A。
考点:考查元素周期表中区的有关判断
点评:该题是基础性试题的考查,也是高考中的常见考点,试题基础性强,侧重对学生基础知识的巩固和训练,主要是考查学生对区的含义以及判断依据的熟悉了解程度,难度不大,记住即可。
本题难度:简单
3、选择题 下列叙述正确的是
A.对于平衡体系:H2(g)+I2(g)═2HI(g),其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深
B.-定温度下,物质的量浓度相同的4种溶液①CH3COONa②NaNO3?③Na2CO3?④NaOH,pH的大小顺序是④>③>①>②
C.O.1mol?L-1的氨水加水稀释后,NH3?H20的电离程度增大,c(OH-)增大,c(H+)减小
D.常温下,的溶液中:Na+、Al3+、SO42-、NO3-可大量共存
参考答案:B
本题解析:分析:A.增大压强,平衡不移动;
B.碱的pH>水解显碱性的pH>不水解的盐溶液的pH,①③中水解程度大的盐溶液的pH大;
C.氨水加水稀释后,促进电离,c(OH-)减小;
D.常温下, 的溶液,c(OH-)=0.01mol/L,溶液显碱性.
的溶液,c(OH-)=0.01mol/L,溶液显碱性.
解答:A.对于平衡体系:H2(g)+I2(g)═2HI(g),其它条件不变时,增大体系压强,平衡不移动,颜色加深,故A错误;
B.定温度下,物质的量浓度相同的4种溶液①CH3COONa②NaNO3?③Na2CO3?④NaOH,碱的pH>水解显碱性的pH>不水解的盐溶液的pH,①③中水解程度大的盐溶液的pH大,则pH的大小顺序是④>③>①>②,故B正确;
C..1mol?L-1的氨水加水稀释后,NH3?H20的电离程度增大,c(OH-)减小,Kw不变,则c(H+)增大,故C错误;
D.常温下, 的溶液,c(OH-)=0.01mol/L,溶液显碱性,Al3+不能大量存在,故D错误;
的溶液,c(OH-)=0.01mol/L,溶液显碱性,Al3+不能大量存在,故D错误;
故选B.
点评:本题考查知识的较多,涉及盐类水解、化学平衡、溶液的pH、弱电解质的电离、离子共存等,注重基础知识的考查,题目难度中等.
本题难度:简单
4、选择题 下列分子中,共价键的极性最强的是
A.NH3
B.H2S
C.CH4
D.H2O
参考答案:D
本题解析:非金属性越强和氢原子形成的共价键极性就越强,非金属性强弱顺序为O>N>S>C,所以答案是D。
本题难度:一般
5、选择题 下列元素中,不属于第ⅠA族的是
A.锂
B.钠
C.镁
D.钾
参考答案:C
本题解析:
本题难度:简单