微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某物质的晶体中含有A、B、C三种元素,其排列方式如图所示(其中前后两面面中心的B元素的原子未能画出)。晶体中A、B、C的原子个数比为
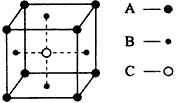
[? ]
A.1∶3∶1
B.2∶3∶1
C.2∶2∶1
D.1∶3∶3
参考答案:A
本题解析:
本题难度:一般
2、选择题 下列数据是对应物质的熔点:
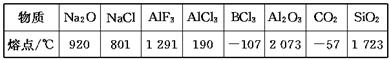
据此做出的下列判断中错误的是(?)
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
参考答案:B
本题解析:据图表我们可以知道分子晶体的熔点比较低,所以氯化铝也是属于分子晶体故B选项是错误的。
本题难度:简单
3、填空题 天然气既是重要的能源,也是重要的化工原料,其主要成分是甲烷。
(1)甲烷在一定条件下可生成:
A.碳正离子(CH3-) ? B.碳负离子(CH3-)
C.甲基(―CH3)?D.碳烯(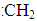 )
)
①四种微粒中,键角为120°的是________。(填序号)
②与碳负离子(CH3-)互为等电子体的一种分子的结构式为_________________________________________________________。
(2)海底富藏大量的可燃冰(甲烷的水合物),关于可燃冰的说法中正确的是________。
A.甲烷分子与水分子均是极性分子
B.可燃冰中甲烷分子与水分子间以氢键相结合
C.可燃冰属于原子晶体
D.甲烷分子与水分子中的σ键均是s―sp3电子云重叠而成的
(3)在高温下,甲烷可还原CuO得到Cu2O。
①Cu+的核外电子排布式为____________。
②Cu2O晶体的晶胞结构如图所示。其中“△”代表的离子符号为________。

(4)一定条件下,甲烷与水蒸气可生成H2和CO。则所生成的气体中σ键总数与π键总数之比为________。
参考答案:(1)①A ② (2)D (3)①[Ar]3d10
(2)D (3)①[Ar]3d10
②O2- (4)2∶1
本题解析:(1)A中碳原子杂化为0+3=3,sp2,平面三角形。B中为1+3=4,sp3杂化,三角锥形。C中为1+3=4,sp3杂化,三角锥形。D中为1+2=3 ,sp2,平面三角形,由于孤电子对斥力大,所以键角小于120°。(2)A项,甲烷分子中正、负电荷中心重合,非极性分子,错误。B项甲烷中C―H无法形成氢键,错误。C项,可燃冰属于分子晶体,错误。(3)中由晶胞可知,黑球为4,白球为1,由于Cu2O,离子个数比为2∶1,可知,中心为氧离子。注意写Cu+,不是铜原子。
本题难度:一般
4、填空题 金属体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点和各个面的中心有一个金原子,每个金原子被相邻的晶胞所共用(下图).金原子的直径为d,用NA表示阿伏加德罗常数的值,M表示金的摩尔质量.
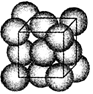
(1)金晶体每个晶胞中含有________个金原子.
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定______________________________________________________________________.
(3)一个晶胞的体积是多少?
(4)金晶体的密度是多少?
参考答案:(1)4
(2)在立方体各个面的对角线上3个金原子两两相切(3)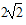 d3
d3
(4)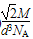
本题解析:
本题难度:一般
5、选择题 厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如下图,它是由C70分子与Cl2发生加成反应得到的。在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形。则有关说法中不正确的是

A.C70的熔点比石墨的熔点低
B.C70和金刚石是同素异形体
C.C70分子中含有70个σ键,35个π键
D.C70Cl10分子中共用电子对数目为145个
参考答案:C
本题解析:C70是由碳元素组成的单质,属于分子晶体,熔点低于石墨的,A正确;C70和金刚石都是碳元素形成的不同单质,互为同素异形体,B正确;在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,每个碳原子有四个未成对电子,分别和其他三个原子成键,所以,有三个碳碳键,四对公用电子对,所以,必然有一条键是双键,因此双键个数是70÷2=35,则单键个数是(70×4-35×4)÷2=70.应用双键是由1个σ键和2个π键构成的,则C70分子中含有105个σ键,35个π键,C不正确;C70Cl10分子中共用电子对数目为145个(70×4+10)÷2=145,则选项D正确,答案选C。
点评:该题是中等难度的试题,试题综合性强,对学生的要求较高,有利于激发学生的学习兴趣和学习积极性,有利于培养学生的逻辑推理能力和抽象思维能力。
本题难度:简单