微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 I.已知几种元素原子的价电子构型为3s2,4s2,4s24p1,3d54s2,3s23p3,它们分别属于第几周期?第几族?最高化合价是多少?各元素符号分别是什么?
Ⅱ.第四周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7,其原子序数依次增大。已知A与B 的次外层电子数均为8,而C与D的次外层电子数均为18。根据原子结构,判断:
(1)A、B、C、D的元素符号分别是________、________、________、________。
(2)写出D与A的简单离子的电子排布式________,________。
(3)哪一种元素的氢氧化物碱性最强?__________________________________________。
(4)B与D两原子间能形成何种化合物?________________。写出化学式及电子式________________,________________。
参考答案:Ⅰ.Mg 第3周期ⅡA族、+2;Ca 第4周期ⅡA族、+2;Ga 第4周期ⅢA族、+3;Mn 第4周期ⅦB族、+7;P 第3周期ⅤA族、+5。
Ⅱ.(1)K? Ca? Zn? Br
(2)Br-:1s22s22p63s23p63d104s24p6 K+:1s22s22p63s23p6
(3)K
(4)离子化合物? CaBr2?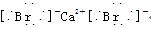
本题解析:Ⅰ.根据价电子构型判断5种元素分别为Mg、Ca、Sc、Mn、P。Ⅱ.
根据A、B、C、D的原子结构判断分别为K、Ca、Zn、Br。
本题难度:一般
2、选择题 下列关于原子半径的周期性变化描述不严谨的是
A.元素 的原子半径随元素原子序数的递增呈周期性变化
的原子半径随元素原子序数的递增呈周期性变化
B.同周期元素随着原子序数的递增,元素的原子半径自左到右逐渐减小
C.同主族元素随着原子序数的递增,元素的原子半径自上而下逐渐增大
D.电子层数相同时,有效核电荷数越大,对外层电子的吸引作用越强
参考答案:B
本题解析:略
本题难度:一般
3、选择题 下列有关14C、14N这两种核素的说法正确的是:
A.质量数不相同? B.电子数相同? C.中子数不相同? D.质子数相同
参考答案:C
本题解析:略
本题难度:简单
4、选择题 电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取(?)
A.电子的运动轨迹图像
B.原子的吸收光谱
C.电子体积大小的图像
D.原子的发射光谱
参考答案:B
本题解析:电子由3d能级跃迁至4p能级时,需要吸收能量,所以选项B正确。答案选B。
本题难度:一般
5、选择题 下列说法正确的是?
A.Li是最活泼金属,F是最活泼非金属
B.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
C.X2+的核外电子数目为18,则X在第四周期第ⅡA族
D.Mg(OH)2碱性比Ca(OH)2强
参考答案:C
本题解析:A选项Fr才是最活泼的金属。故A选项是错误的。B选项在周期表中,有7个横行,7个周期,有18个纵行,16族。因此B选项是错误的。D半径越大,碱性越强,钙的半径比镁的大,因此氢氧化钙的碱性比氢氧化镁的强,所以D选项是错的
本题难度:一般