��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽΪ��
A��FeCl3��Һ��Cu�ķ�Ӧ��Cu��Fe3����Cu2����Fe2��
B��NH4HCO3���ڹ�����NaOH��Һ�У�HCO3-+OH-=CO32-+H2O
C������ʯ���ڴ����У�CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2��+H2O
D����AlCl3��Һ�м��������ˮ��Al3����3OH����Al(OH)3��
�ο��𰸣�C
���������A����ɲ��غ㡣
B�����ڰ������������������ӵķ�Ӧû��д������
C��ȷ��
D����AlCl3�백ˮ��Ӧ�������������������������Dz���������ġ�������ȷѡ����C��
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A����Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO4-+6H++5H2O2=2Mn2++5O2��+8H2O
B��������SO2ͨ�뱽������Һ�У�2C6H5O-+SO2+H2O=2C6H5OH+SO32-
C�������軯����Һ���Լ�����Һ�е�Fe3+��Fe3++3SCN-=Fe��SCN��3��
D����⻯������Һ��ͨ�������������2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
�ο��𰸣�A����Ũ�����ữ���������Һ��Ӧ��Ũ���������ط���������ԭ��Ӧ����ȷ�����ӷ���ʽΪ2MnO4-+16H++10Cl-�T2Mn2++5Cl2��+8H2O
����A����
B�������������ǿ�ڱ��ӣ�ǿ�������ᣬ��ȷ�����ӷ���ʽΪ2C6H5O-+SO2+H2O=2C6H5OH+SO32-����B��ȷ��
C�����軯���ǿ�����ˮ��������ȷ�����ӷ���ʽΪFe3++3SCN-=Fe��SCN��3����C����
D���⻯������Һ��ͨ������������������Ӻ���������Ҫ�������֮�ȣ���ȷ�����ӷ���ʽΪ2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-����D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ�У���д����ȷ����?��?��?
A���Ȼ�����Һ�м�����������Һ��Ag+ + Cl- = AgCl��
B���ѽ����Ʒ���ˮ�У�Na + 2H2O =" Na+" +2OH- + H2
C������ˮ����⻯����Һ�У�Cl2 + 2I- ="" 2Cl- + I2
D���������ʯ��ʯ�ϣ�CaCO3 + 2H+ =" Ca2+" + CO2�� + H2O
�ο��𰸣�B
�����������
�����Ѷȣ���
4��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
[? ]
A�������������봿�Ӧ��2Al3++3CO32-+3H2O=2Al(OH)3��+3CO2��
B������ͭ���ռӦ��CuSO4+2OH-=Cu(OH)2��+SO42-
C��������̼���Ʒ�Ӧ��2C6H5OH+CO32-=2C6H5O-+CO2��+H2O
D��̼�ᱵ�����ᷴӦ��Ba2++SO42-=BaSO4��
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5��ѡ���� ����˵���������ȷ���ǣ�?��
�ٻ���̿��SO2��HClO������Ư�����ã���Ư�Ļ�ѧԭ����ͬ
����100mL0.1mol/L ���廯������Һ��ͨ��0.05mol������ʱ������Ӧ�����ӷ���ʽ��
2Fe2����4Br-��3Cl2="2" Fe3����2Br2��6Cl-
����Ϊ�����ԣ�HClO��ϡH2SO4�����Էǽ����ԣ�Cl��S
������������KIO3��Һ��KI��Һ������Ӧ����I2ʱ�����ӷ���ʽ��
IO3����5I����3H2O=I2��6OH��
��̼��������ӵĵ��뷽��ʽ�ɱ�ʾΪ��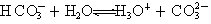
��Ԫ�����ڱ��У����ϵ��£�±��Ԫ�صķǽ�������������±����������μ���
��500�桢30MPa�£���0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3kJ�����Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)  2NH3 (g) ?��H=-38.6kJ��mol-1
2NH3 (g) ?��H=-38.6kJ��mol-1
A��ȫ��
B���ڢ�
C���ڢۢܢ�
D���ڢܢ�
�ο��𰸣�B
����������ٻ���̿��Ư�����������ã����������仯��HClO��Ư����������HClO��ǿ�����ԣ�SO2��Ư����SO2������ɫ�����ʷ����˷�������Ӧ��������ɫ���ʣ�Ư��ԭ����ͬ������FeBr2��Cl2�����ʵ���֮��Ϊ1:5��Cl2���������ӷ���ʽ��ȷ����HClO��ϡ�����������ǿ���ͷǽ������أ��������������£�����������OH?���������ɵ�H3O+ΪH+����ȷ����Ԫ�����ڱ��У����ϵ��£���±�������������ǿ��������ΪN2��H2�ķ�ӦΪ���淴Ӧ������0.5mol N2��1.5mol H2��������ȫ��Ӧ��������?H������
�����Ѷȣ�һ��