微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 为验证Cl2、Br2的氧化性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如下图,填写图中的空白。
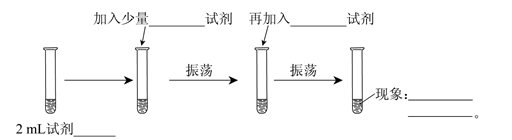
(1)2 mL 试剂 ;加入少量 试剂;再加入
试剂; 现象: & #160; 。
(2)可以证明Cl2的氧化性____________(填“强于”或“弱于”)Br2的氧化性;氯元素的非金属性 ____________(填“强于”或“弱于”)_溴元素的非金属性。
( 3 )此反应的离子方程式为:________________________________________。
(4)某溶液中Cl-、Br-、I-的物质的量之比为4∶1∶4,要使溶液中的Cl-、Br-、I-的物质的量之比变为7∶1∶1,则通入Cl2的物质的量与原溶液中I-的物质的量之比为______。
参考答案:(1)NaBr溶液 ; 氯水 ; 四氯化碳 ; 分成两层 上层无色、下层棕红色(或橙色或橙红色) 。
(2)强于;强于(3)Cl2+2Br-=2Cl-+Br2
(4)3:8
本题解析:(1)验证Cl2、Br2的氧化性强弱,结合题干提供的试剂,可知第一支试管应该装的是2mLNaBr溶液,第二支试管中加入氯水,振荡之后再加入CCl4把置换出来的Br2从混合液中萃取出来,混合液分成两层,上层为NaCl溶液无色,下层Br2和CCl4,呈棕红色(或橙色或橙红色)。
(2)由实验证明Cl2的氧化性强于Br2的氧化性,结合元素周期律,也可得氯元素的非金属性强于溴元素的非金属性。该反应的离子方程式为:Cl2+2Br-=2Cl-+Br2 。
(4)依题意,可设原溶液中Cl-、Br-、I-的物质的量为4X、X、4X,反应后溶液中的Cl-、Br-、I-的物质的量为7X、X、X,通入氯气后,发生如下反应:Cl2+2I-=2Cl-+I2,可知I-的减少量为Cl2通入量的2倍,则 ,
,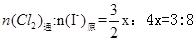 。
。
考点:化学实验,卤素的化学性质,物质的量计算。
点评:探究式实验是近年来高考的热点,重在培养学生的发散性思维,逻辑思维能力,本题难度不大,解题的关键是要掌握卤素的化学性质和反应方程式的正确书写,结合反应原理,题干信息,巧妙假设,化繁为简。
本题难度:困难
2、实验题 某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
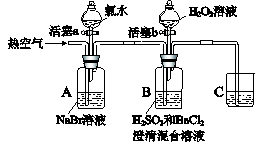
实验记录如下:
?
| 实验操作
| 实验现象
|
I
| 打开活塞a,滴加氯水,关闭活塞a
| A中溶液变为红棕色。
|
II
| 吹入热空气
| A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化。
|
III
| 停止吹入空气,打开活塞b,逐滴加入H2O2溶液
| 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色。
|
?
请回答下列问题:
(1)A中反应的离子方程式是?。
(2)实验操作II吹入热空气的目的是?。
(3)装置C的作用是?,C中盛放的药品是?。
(4)实验操作III,混合液逐渐变成红棕色,其对应的离子方程式?。
(5)由上述实验得出的结论是?。
(6)实验反思:
①有同学认为实验操作II吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是?。
②实验操作III,开始时颜色无明显变化的原因是(写出一条即可):?
?。
参考答案:(16分,每空2分)
(1)2Br-+Cl2=Br2+2Cl-
(2)吹出单质Br2
(3)吸收尾气? NaOH溶液
(4)H2O2+2Br-+2H+=Br2+2H2O
(5)氧化性:H2O2>Br2>H2SO3
(6)
① 不干扰,无论热空气是否参加氧化H2SO3,只要观察到产生白色沉淀的同时无明显颜色变化,即能证明Br2氧化了H2SO3
② H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可)
本题解析:(1)氯水中的Cl2置换Br?。
(2)利用Br2的挥发性,吹入热空气使Br2挥发。
(3)因为Cl2、Br2有毒,所以C中盛放NaOH溶液,除去尾气中的有毒气体,防止污染环境。
(4)混合液逐渐变成红棕色,说明H2O2把Br?氧化为Br2,配平可得离子方程式。
(5)根据氧化剂的氧化性大于氧化产物,可知:H2O2>Br2>H2SO3。
(6)①溶液无明显颜色变化,说明Br2参加了反应,即氧化了H2SO3。
②实验操作III发生的反应为H2O2氧化Br?,开始时颜色无明显变化,说明反应收到了影响,H2SO3有剩余、H2O2浓度小、Br-与H2O2反应慢等都是可能因素。
本题难度:困难
3、选择题 已知:
①2BrO3-+Cl2=Br2+2ClO3-;
②5Cl2+I2+6H2O=2HIO3+10HCl;
③ClO3-+5Cl-+6H+=3Cl2↑+3H2O
下列按物质氧化性顺序由强到弱排列正确的是( )
A.Cl2>BrO3->ClO3->IO3-
B.BrO3->ClO3->Cl2>IO3-
C.ClO3->BrO3->IO3->Cl2
D.BrO3->Cl2>ClO3->IO3-
参考答案:①反应2BrO3-+Cl2=Br2+2ClO3-,氧化剂为Cl2,还原剂为BrO3-,所以氧化性BrO3->ClO3-;
?②5Cl2+I2+6H2O=2HIO3+10HCl,氧化剂为Cl2,氧化产物为IO3-,所以氧化性Cl2>IO3-;
③ClO3-+5Cl-+6H+=3Cl2↑+3H2O,氧化剂为ClO3-,氧化产物为Cl2,所以氧化性ClO3->Cl2;
所以氧化性BrO3->ClO3->Cl2>IO3-.
故选B.
本题解析:
本题难度:简单
4、选择题 含有a mol FeBr2的溶液中,通入 x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是 (? )
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,2Br-+Cl2=Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
参考答案:B
本题解析:Fe2+的还原性比Br-强,所以Cl2通入FeBr2溶液中,当Cl2不足量时,会先与Fe2+反应;待Fe2+全部被氧化成Fe3+后,过量的Cl2才会与Br-反应。
本题目中,反应前Fe2+物质的量为amol,而amol的Fe2+被氧化需要消耗掉0.5amolCl2,即x<0.5a时,该反应的离子方程式为Cl2+2Fe2+=2Cl-+2Fe3+所以说法A是正确的。
当x>0.5a时,Cl2开始与Br-反应。所以说法B是错误的。
纵观说法C与D中的离子方程式,都是由说法A与B中的两个离子方程式相加而成的。只是说法C中,除了0.5amolCl2与Fe2+反应完成后,另0.5amol的Cl2继续与amol的Br-发生反应,但仍有amolBr-未参与反应。说法D中Cl2恰好与所有的Fe2+和Br-反应完全。所以这两个离子方程式都不能说是错误的。2和氯气的反应
点评:本题考查FeBr2和氯气的反应,解答本题关键要在于了解Fe2+的还原性比Br-强,所以Cl2通入FeBr2溶液中,当Cl2不足量时,会先与Fe2+反应;待Fe2+全部被氧化成Fe3+后,过量的Cl2才会与Br-反应。
本题难度:一般
5、填空题 已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去,发生的反应:2MnO4- +16H+ + 10Cl- === 2Mn2+ + 5Cl2↑ + 8H2O。现有一个氧化还原反应中,已知反应物和生成物有KCl、H2SO4、
KMnO4、MnSO4、H2O、K2SO4、Cl2。
(1)已知该反应中,KMnO4得到电子,写出一个包含上述七种物质的氧化还原反应方程式(不需要配平)
_____________________________;则反应的还原剂为________________
(2)上述反应中,1mol氧化剂在反应中得到__________电子
(3)如果在反应后的溶液中加入NaBiO3,溶液又变回紫红色,请判断下列正确的是____________
A.氧化性:BiO3->MnO4->Cl2 B.氧化性:BiO3->Cl2>MnO4-
C.氧化性:MnO4->BiO3->Cl2 D.氧化性:Cl2>MnO4->BiO3-
参考答案:(1)KCl+KMnO4+H2SO4→MnSO4+K2SO4+Cl2↑+H2O;KCl
(2)5mol
(3)A
本题解析:
本题难度:一般