| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ�����������ǽ������ϡ�����Ԥ�⣨2017�����°棩(��)
A��A B��B C��C D��D �ο��𰸣�C ��������� �����Ѷȣ��� 4������� ���ֺ���Ԫ�ص�����֮����ת����ϵ��ͼ��ʾ�� �ο��𰸣���1��AΪ����Ԫ�ص����ʣ�A�ܺͼӦ����Ϊ���������赥�ʣ�B�ܺ�̼���ʷ�Ӧ����A������Aֻ���ǹ赥�ʣ�B�ܺ������Ʒ�Ӧ���ܺ���̼��Ʒ�Ӧ������BΪ�������裬��������������Ʒ�Ӧ���ɹ����ƣ�����DΪ�����ƣ��ҹ���������Ʒ�Ӧ����D����һ����֤AΪ�裬BΪ�������裬��������Һ��ͨ�������̼������Fԭ���������Fԭ�������õ�����C���������ȷֽ�õ�BΪ�������裬��һ�εõ���֤��BΪ���������̼��Ʒ�Ӧ���ɹ���ƣ�����EΪ����ƣ� ��������� �����Ѷȣ�һ�� 5������� ��12�֣�CoCl2��6H2O��һ������Ӫ��ǿ������һ������ˮ�ܿ�[��Ҫ�ɷ�ΪCo2O3��Co(OH)3����������Fe2O3��Al2O3��MnO��]��ȡCoCl2��6H2O�Ĺ����������£�
(2)NaClO3��������?�� (3)��Na2CO3��pH��5.2���ó���Ϊ?�� (4)��ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ����ȡ����������?����ʹ�õ�����pH��Χ��?�� A��2.0~2.5? B��3.0~3.5? C��4.0~4.5 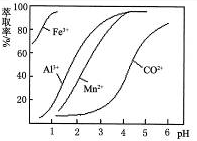 ��5��Ϊ�ⶨ�ֲ�Ʒ��CoCl2��6H2O��������ȡһ�������Ĵֲ�Ʒ����ˮ����������AgNO3��Һ�����ˡ�ϴ�ӣ���������ɺ����������ͨ�����㷢�ֲִ�Ʒ��CoCl2��6H2O��������������100������ԭ�������?������һ�����ɣ� �ο��𰸣���12�֣� ����������� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ����������.. | |
| �����Ŀ |