| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《盐类水解的原理》高频试题强化练习(2017年最新版)(十)
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管 |
参考答案:
Ⅰ:N2(g)+3H2(g)=2NH3(g) ΔH=-92kJ・mol-1
Ⅱ:
【小题1】Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊 应加入少量H2SO4 【小题2】2Al3++3S2-+6H2O = 2Al(OH)3↓+3H2S↑
III:
【小题1】溶液由浅绿色变为紫红色,且半分钟后不变则达到滴定终
【小题2】C
【小题3】ABDE
【小题4】50%
本题解析:Ⅰ:考查反应热的计算和热化学方程式的书写。反应热就是断键吸收的能量和相差化学键放出的能量的差值。因此该反应的反应热为3×436kJ/mol+9466kJ/mol-2×3×3916kJ/mol=-926kJ/mol,因此反应的热化学方程式为N2(g)+3H2(g)=2NH3(g) ΔH=-92kJ・mol-1。
Ⅱ:硫酸铜属于强酸弱碱盐,在溶液中铜离子水解生成氢氧化铜和硫酸。因为水解是吸热的,加热促使水解平衡向正反应方向移动,生成氢氧化铜沉淀,所以溶液会产生混浊。要想不产生混浊,则必须抑制铜离子的水解,因为水解显酸性,所以可以加入少量硫酸以抑制水解。
III:考查基本实验操作和有关计算。
(1)因为高锰酸钾溶液是显紫红色的,当溶液中的亚铁离子被完全氧化生成铁离子后,如果再加一滴酸性高锰酸钾溶液,则溶液的颜色将显紫红色,据此可判断终点。
(2)选项A中相当于稀释了标准液,则消耗标准液的体积将偏大,测定结果偏高。锥形瓶在滴定实验中是不允许用标准液润洗的,B的操作是正确的。滴定管的刻度自上而下是逐渐增大的,滴定前平视,读数不影响。滴定到终点后俯视,则读数将偏低,因此消耗的标准液体积偏低,测定结果偏低。选项D中相当于把这一滴液体计算到标准液中,实验测定结果偏高。
(3)样品需要称量和溶解并配制溶液,所以A、B、D均需要。酸性高锰酸钾溶液具有强氧化性,需要放在酸式滴定管中,D需要。
(4)根据实验可知消耗高锰酸钾是10.00ml,根据方程式可知10.0ml待测液中硫酸亚铁的物质的量是5×0.01L×0.1mol/L=0.005mol。所以FeSO4的质量分数为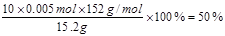 。
。
本题难度:困难
2、选择题 氯化铵晶体溶于重水(D2O)中,溶液呈现酸性,下列叙述的原因中正确的是
A.NH4+水解生成NH3・H2O和HD2O+
B.NH4+水解生成NH3・DHO和HD2O+
C.NH4+水解生成NH3・D2O和HD2O+
D.NH4+水解生成NH3・DHO和D3O+
参考答案:D
本题解析:氯化铵是强酸弱碱盐,NH4+水解显酸性。水解的实质是NH4+结合水电离出的OH-生成一水合氨,在重水中则结合OD-生成NH3・DHO。在重水中氢离子是以D3O+形式存在。所以正确的答案是D。
本题难度:困难
3、选择题 等体积等物质的量浓度MOH强碱和HA弱酸溶液混合后,混合液中有关离子浓度应满足的关系 是
A.c(M+)>c(H+)>c(A-)>c(OH-)
B.c(M+)>c(A-)>c(OH-)>c(H+)
C.c(M+)>c(OH-)>c(A-)>c(H+)
D.c(M+)>c(A-)>c(H+)>c(OH-)
参考答案:B
本题解析:等体积等物质的量浓度MOH强碱和HA弱酸溶液混合后,生成的MA盐是强碱弱酸盐,A-水解显碱性,离子浓度关系为c(M+)>c(A-)>c(OH-)>c(H+) ,选B。
考点:盐类水解和溶液中离子浓度的大小
本题难度:困难
4、选择题 将0.2mol/L HCN溶液和0.1mol/L NaOH溶液等体积混合后溶液呈碱性,下列关系式中不正确的是
A.c(HCN) >c(CN―)
B.c(Na+)>c(CN―)
C.c(HCN)-c(CN―)=c(OH―)
D.c(HCN)+c(CN―)=0.1mol/L
参考答案:C
本题解析:将0.2mol/L HCN溶液和0.1mol/L NaOH溶液等体积混合后,得到0.05mol/L NaCN和0.05mol/L HCN的混合溶液,溶液存在HCN H++ CN―,CN―+H2O
H++ CN―,CN―+H2O OH―+HCN,溶液呈碱性,说明水解大于电离,c(HCN) >c(CN―),故A正确;根据电荷守恒,c(Na+)+ c(H+) >c(CN―)+ c(OH―) ,溶液呈碱性,c(Na+)>c(CN―),故B正确;c(HCN)-c(CN―)=2c(OH―)-2 c(H+) ,故C错误;c(HCN)+c(CN―)=0.1mol/L符合物料守恒,故D正确。
OH―+HCN,溶液呈碱性,说明水解大于电离,c(HCN) >c(CN―),故A正确;根据电荷守恒,c(Na+)+ c(H+) >c(CN―)+ c(OH―) ,溶液呈碱性,c(Na+)>c(CN―),故B正确;c(HCN)-c(CN―)=2c(OH―)-2 c(H+) ,故C错误;c(HCN)+c(CN―)=0.1mol/L符合物料守恒,故D正确。
考点:本题考查盐的水解。
本题难度:一般
5、填空题 (1)向FeCl3溶液中投入适量的Zn粉,会有 放出(填化学式)。
(2)室温下,向氨水中滴加盐酸,当溶液呈中性时,C(NH4+) C(Cl- )(填< 或>或=)
(3)盐的水解反应为吸热反应,升高温度水解程度 (填增大或减小或等于)
(4)写出Na2CO3溶液中的电荷守恒式
参考答案:(1)H2。(2)== (3)增大
(4)c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-)
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《物质的量》.. | |