��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʵ����Ƽ����Ӧ�����ӷ���ʽ����ȷ���ǣ�?��
A����FeCl3��Һ��ʴͭ��·�壺Cu + 2Fe3+="===" Cu2+ + 2Fe2+
B��Na2O2��H2O��Ӧ�Ʊ�O2��Na2O2 + H2O==== 2Na+ + 2OH��+ O2��
C����NaAlO2��Һ��ͨ�����CO2��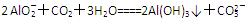
D��NaHCO3��ˮ�⣺HCO3����H2O H3O����CO32��
H3O����CO32��
�ο��𰸣�A
���������A��ȷ��B����ȷ��û����ƽ��Ӧ����2Na2O2 + 2H2O��4Na+ + 4OH��+ O2����C����ȷ����ΪCO2�ǹ����ģ��������Ӧ����̼�����ƣ�������̼���ƣ�D����ȷ���÷�Ӧ�ǵ���ƽ�⣬ˮ�ⷽ��ʽӦ����HCO3����H2O H2CO3��OH������ѡA��
H2CO3��OH������ѡA��
�����������Ǹ߿��еĸ�Ƶ�⣬�����е��Ѷȵ����⣬���ض�ѧ��������������ѵ����������Ҫ��ȷ�ж����ӷ���ʽ��ȷ���ķ���һ�㣬����1����鷴Ӧ�ܷ�������2����鷴Ӧ��������Ƿ���ȷ����3���������ʲ���Ƿ���ȷ����4������Ƿ�����غ��ϵ���磺�����غ�͵���غ�ȣ�����5������Ƿ����ԭ��ѧ����ʽ��Ȼ��������ü��ɡ���������������ѧ���������⡢��������������
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A��������������Һ�к�������Һ��Ba2++OH-+H++SO42-=H2O+BaSO4��
B��������������Һ��ӦFe3++Fe�T2Fe2+
C���Ȼ�����Һ�м��������ˮAl3++4OH-=AlO2-+2H2O
D������������ˮ��Ӧ2Na2O2+2H2O=4Na++4OH-+O2��
�ο��𰸣�A��������������Һ�к�������Һ�ķ�ӦΪBa2++2OH-+2H++SO42-=2H2O+BaSO4������A����
B�����ӷ�Ӧ��Ӧ��ѭ����غ㣬��������������Һ�����ӷ�ӦΪ2Fe3++Fe�T3Fe2+����B����
C���Ȼ�����Һ�м��������ˮ�����ӷ�ӦΪAl3++3NH3��H2O�TAl��OH��3��+3NH4+����C����
D������������ˮ��Ӧ�����ӷ�ӦΪ2Na2O2+2H2O=4Na++4OH-+O2������D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� ��ʧȥ��ǩ��A��B��C��D��ƿ��Һ�����ǵijɷֿ�����Na2CO3��K2SO4��Ba(NO3)2��NaHSO4�е�ijһ�֣���������ʵ�飺
��1��A+C����Һ��+�����?��2��B+A����Һ��+������
��3��C+B����Һ��+������?��4����Һ��+�����١���Һ��+�����
��������ʵ������д���������̵����ӷ���ʽ��
��1��?��
��2��?��
��3��?��
��4��?��
�ο��𰸣���1��2H++CO32�� ��CO2��+H2O?��2��CO32��+ Ba2+ ��BaCO3��
��3��Ba2++SO42�� ��BaSO4��?��4��BaCO3+2H+ ��Ba2+ +CO2��+H2O
���������B��A��C��϶��г������������BӦΪBa(NO3)2��A��C������������ɣ���˵������Ӧ����̼���ƺ��������ƣ���D������ء�������������Һ�ۻ�ϣ������ܽⲢ������ζ����˵���ó���һ����̼�ᱵ������A��̼���ƣ���C���������ơ���˷�Ӧ�е��й����ӷ�Ӧ����ʽ�ֱ���2H++CO32�� ��CO2��+H2O��CO32��+ Ba2+ ��BaCO3����Ba2++SO42�� ��BaSO4����BaCO3+2H+ ��Ba2+ +CO2��+H2O��
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��д��ȷ����?
A�����������Һ��ͨ������Ķ�����̼��SiO32����CO2��H2O��H2SiO3����CO32��
B�����Ȼ�����Һ�м�������İ�ˮ��Al3+ +4NH3��H2O��AlO2��+4NH4++2H2O
C�������ʯ��ˮ�еμӹ���̼�������Һ��Ca2+��HCO3����OH����CaCO3����H2O
D��������������Һ�м���ϡ���Fe2++4H++NO3�� ="=" Fe3++NO��+2H2O
�ο��𰸣�C
���������������һ���߿��еij������⣬�Կα��ϳ��ֵĻ�ѧ��ӦΪ��������ѧ�������ӷ���ʽ��д�����������A��ͨ������Ķ�����̼�����ܴ���CO32����B�а�ˮ��������ܽ�Al(OH)3, D ��ɲ�ƽ��
�����Ѷȣ�һ��
5��ѡ���� ����������ʵ�뻯ѧ�������ӣ�����ʽ���������?��?��
A����˵��NH3���H+������H2Oǿ��N H3+H2O
H3+H2O NH4++OH-
NH4++OH-
B����˵��������H2O2>Fe3+��2Fe2++H2O2+2H+=2Fe3++2H2O
C����˵����������Ա�̼��ǿ��2HCl+CaCO3=CaCl2+H2O+CO2��
D����˵��CH3COPH�����CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
�ο��𰸣�A
�����������
�����Ѷȣ�һ��