微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A、B是短周期VIIA族的两种元素,A的非金属性比B强。下列关于A、B的说法正确的是
A.A元素的单质可以把B元素的单质从NaB溶液中置换出来
B.NaA、NaB的晶体都是离子晶体,且NaA晶体的熔点比NaB高
C.HA的沸点比HB高,是因为1mol HA分子中H-A键断裂时吸附的能量比1mol
HB分子中H-B键断裂时吸收的能量多
D.常温下,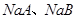 溶液的pH均大于7
溶液的pH均大于7
参考答案:B
本题解析:A、A、B是短周期VIIA族的两种元素,A的非金属性比B强,则A为F元素,B为Cl元素,F2与NaCl溶液反应,实际反应为F2与H2O反应生成O2,错误;B、短周期VIIA族为活泼非金属,与Na元素结合的化合物为离子化合物,F?半径小于Cl?半径,则NaF的晶格能大于NaCl的晶格能,所以NaF晶体的熔点比NaCl高,正确;C、HF的沸点比HCl的沸点高,是因为HF分子间形成了氢键,作用力大于HCl分子间的范德华力,错误;D、因为NaCl为强酸强碱盐,所以常温下,NaCl溶液的pH等于7,错误。
本题难度:一般
2、选择题 下列说法正确的是(?)
A.H2O是一种非常稳定的化合物,这是由于氢键所致
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属晶体的熔点普遍都很高
参考答案:B
本题解析:氢键一般影响物质的物理性质,水分子稳定,是由于化学键的原因。干冰升华属于物理变化,破坏的是分子间作用力。金属晶体的熔点并不都是普遍很高,例如碱金属等。所以正确的答案是B。
本题难度:一般
3、选择题 下列关于化学键的说法正确的是( )
①含有金属元素的化合物一定是离子化合物
②第IA族和第VIIA族原子化合时,一定生成离子键
③由非金属元素形成的化合物一定不是离子化合物
④活泼金属与非金属化合时,能形成离子键
⑤离子键就是阴、阳离子间的静电引力
⑥含有离子键的化合物一定是离子化合物
⑦离子化合物中可能同时含有离子键和共价键.
A.①②⑤
B.④⑥⑦
C.①④③
D.②③⑤
参考答案:B
本题解析:
本题难度:一般
4、选择题 有关化学用语正确的是( )
A.甲烷的结构简式CH4
B.羟基的电子式
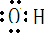
C.异戊烷的分子式C5H8
D.乙烯的结构简式CH2CH2
参考答案:A
本题解析:
本题难度:简单
5、填空题 (10分)甲、乙、丙、丁为前三周期元素形成的微粒,它 们的电子总数均为14。
们的电子总数均为14。
已知:甲为原子;乙、丙、丁为双 原子分子或离子。
原子分子或离子。
⑴甲单质与氢氧化钠溶液反应的离子方程式为 ? ? ? ;
⑵乙是双原子分子,在高温时是一种还原剂。14 g乙燃烧放出的热量是141.5 kJ。写出乙燃烧的热化学方程式?。
⑶丙为双原子二价阴离子,与钙离子组成的化合物能跟水反应产生一种可燃性气体。该可燃性气体能与乙酸在一定条件下,按物质的量比1∶1发生加成反应生成一种酯,该化学方程式是为?。
⑷由丁分子组成的物质属于单质,组成丁的元素最高价氧化物对应的水化物X有下图所示转化关系(反应条件和其他物质已略)
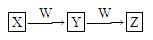
已知W为金属单质,W在周期表中的位置 ? ? 。
写出X的稀溶液与Z反应的离子方程式:?。
参考答案:
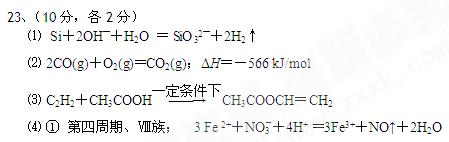
本题解析:略
本题难度:一般