微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有两种气态烷烃的混合物,在标准状况下,其密度为1.16 g・L-1,则关于此混合物组成的说法正确的是( )
A.一定有甲烷
B.一定有乙烷
C.可能是甲烷和己烷的混合物
D.可能是乙烷和丙烷的混合物
参考答案:A
本题解析:混合气体的平均摩尔质量是M(平均)= 1.16 g・L-1×22.4L/mol=26g/mol。在烷烃中相对分子质量小于26的只有甲烷。因此一定含有甲烷。故选项是A。
本题难度:一般
2、实验题 化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。有机物M(分子式:CxHySz)是隐形飞机上吸波材料的主要成分。
M充分燃烧的产物为三种氧化物,写出化学方程式:_______?_______。
Ⅰ定性实验:
某化学兴趣小组为验证M组成元素进行了下列实验:将少量样品放入燃烧管A中,通入一定量O2,用电炉加热使其燃烧,所需装置如图所示(夹持仪器的装置已略去)。

(1)该实验装置连接顺序为____________________。(上述每一组仪器只能使用一次)
(2)D中盛放的试剂是________
(3)能证明有机物含碳元素的现象是_________________________________________。
(4)燃烧管中放入CuO的作用是________________________________。
(5)指出上述中错误的装置:__________________________________________________。
Ⅱ定量实验:
(1)若测产生CO2气体体积,采用如图所示装置,实验结束后①调整量筒内外液面高度使之相同;②冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是:________(请填写步骤代号)。

(2)若测产生CO2气体质量,采用沉淀法。下列沉淀剂最好的是?
a.0.1mol/LCaCl2溶液? b.0.1mol/L Ca(OH)2溶液
c.0.1mol/L Ba(NO3)2溶液? d.0.1mol/L Ba(OH)2溶液
参考答案: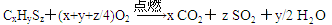
I(1)A、C、B(或D)、D(或B)、E
(2)酸性高锰酸钾溶液
(3)D(或B)中溶液不退色,E中溶液变浑浊
(4)将有机物中的碳元素全部氧化为二氧化碳
(5)装置E中试剂瓶未与空气相通
II(1)②①③(2)d
本题解析:据题意有机物M的分子式为CxHySz,充分燃烧的产物为三种氧化物即CO2、SO2、H2O,据此书写燃烧方程式。
I、根据题意可知,首先应将样品放入A中通氧气氧化,产物中含有CO2、SO2、H2O等,用品红或酸性高锰酸钾溶液检验并吸收SO2,用澄清石灰水检验CO2,所以装置连接顺序为A、C、B、D、E或A、C、D、B、E,D中盛放的试剂是酸性高锰酸钾溶液,证明有机物含碳元素的现象为D(或B)中溶液不退色,E中溶液(澄清石灰水)变浑浊;燃烧管中放入CuO的作用是将有机物中的碳元素全部氧化为二氧化碳;装置中的错误:装置E中试剂瓶未与空气相通。
II、(1)测定产生CO2气体的体积,首先应将产生的气体冷却至室温,然后调整量筒内外液面高度使之相同以减小误差,最后读数。(2)所给四种试剂中,bd均可与CO2生成沉淀,但由于BaCO3的摩尔质量更大,则测定误差相对较小,故最佳沉淀剂为d。
本题难度:简单
3、实验题 (9分)乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全。有关物质的沸点见下:
物质
| 乙醛
| 乙酸
| 甘油
| 乙醇
| 水
|
沸点/℃
| 20.8
| 117.9
| 290
| 78.2
| 100
|
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)
_________________________________________。
(2)如图所示,在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温
度计水银球的位置应在________;当试管A内的主要反应完成后温度计水银球的位置应在_______。

(3)烧杯B内盛装的液体可以是_______。
(4)试管C中收集到的是粗产品,若想进一步提纯,可采用的方法是_____;
提纯后的产品若在质谱仪中进行测定,其质荷比最大是____(填数值);
若在核磁共振仪中进行测定,其核磁共振氢谱共有__种峰,峰面积之比为__。
参考答案:(1)2CH3CHO+O2 2CH3COOH。
2CH3COOH。
(2)浸入试管A的反应液中。试管A的支管口处。
(3)甘油。 (4)蒸馏;60;2;3:1或1:3。
本题解析:(1)在加热并有从;催化剂的条件下乙醛可发生氧化反应生成乙酸,方程式为2CH3CHO+O2 2CH3COOH。
2CH3COOH。
(2)反应开始阶段,需要控制溶液的温度,所以应插入溶液中。当反应结束后需要通过蒸馏分离乙酸,才是需要控制蒸汽的温度,所以应放在试管A的支管口处。
(3)因为乙酸的沸点大于100℃,所以烧杯内液体的温度就必须大于乙酸的沸点,根据表中数据可知需要用甘油。
(4)生成的乙酸会混有没有反应的乙醛,而乙醛的沸点和乙酸的差别很大,所以可以继续通过蒸馏得到乙酸。根据乙酸的分子式CH3COOH可知质荷比最大是是60.乙酸分子中含有2中不同类型的氢原子,其个数比为3:1或1:3。
本题难度:一般
4、选择题 下列操作正确的是(?)
A.配制银氨溶液:在一定量AgNO3溶液中,滴加氨水至沉淀恰好溶解
B.配制Cu(OH)2悬浊液:在一定量CuSO4溶液中,加入少量NaOH溶液
C.制溴苯时,为了充分吸收HBr,将导气管插入水中
D.制取乙酸乙酯实验中,在一定量浓硫酸中,依次加入乙酸和乙醇后加热
参考答案:A
本题解析:B不正确,氢氧化钠应该是过量的;溴化氢极易溶于水,如果将导管直接插入水中,容易造成倒吸,C不正确;制取乙酸乙酯实验中,在一定量乙醇中,慢慢加入浓硫酸和乙酸,D不正确,答案选A。
本题难度:一般
5、填空题 某链状有机物A 4.4g,完全燃烧后只生成4.48LCO2(标准状况)和3.6g水。相同条件下A蒸气的密度为H2的44倍。A与稀H2SO4共热可生成两种有机物甲和乙,甲可发生银镜反应,乙经催化氧化后生成丙,丙不能发生银镜反应。B是A的同分异构体,且B的水溶液显酸性。
请按要求填空:
⑴A的分子式?
⑵乙的结构简式?
⑶B所有可能的结构简式?
参考答案:(1)C4H8O2?(2) ?(3)CH3CH2CH2COOH?
?(3)CH3CH2CH2COOH?
本题解析:(1)4.48LCO2(标准状况)和3.6g水分别都是0.2mol,其中碳氢原子的质量分别是2.4g和0.4g,所以A中移动含有氧原子,质量是4.4g-2.4g-0.4g=1.6g,物质的量是0.1mol,则A的最简式为C2H4O。又因为A蒸气的密度为H2的44倍,所以A的相对分子质量是88,所以A的分子式为C4H8O2。
(2)根据A可以水解可知,A是酯类。甲可发生银镜反应,乙经催化氧化后生成丙,丙不能发生银镜反应,所以甲是甲酸,乙是2-丙醇,丙是丙酮。
(3)分子式相同,而结构不同的化合物互为同分异构体,B显酸性,说明含有羧基,所以B的所有可能结构简式为CH3CH2CH2COOH? 。
。
本题难度:简单