��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ���ǣ�������
A��Ħ����һ�ֹ��ʻ���������
B����״��������Ħ�����ԼΪ22.4L
C��1mol��������Ϊ16g
D��1molH2O������Ϊ18g
�ο��𰸣�D
���������
�����Ѷȣ���
2�������� (������2)Ϊ�ⶨһ�ָ�����������Ĵ��Է�ĩ���ϵ���ɣ���ȡ12.52 g����Ʒ������ȫ���ܽ��ڹ�����ϡ��������100 mL��Һ��ȡ��һ�룬���������K2SO4��Һ�������˰�ɫ�����������ˡ�ϴ�ӡ���ɺ��4.66 g ���塣�����µ�50 mL��Һ�м�������KSCN��Һ���Ժ�ɫ�����������NaOH��Һʱ�����ɺ��ɫ���������������ˡ�ϴ�ӡ����պ��3.20 g���塣
��1��������Է�ĩ����Ԫ�ص���������_____________________��
��2��ȷ���ò��ϵĻ�ѧʽ__________________________________��
����ʾ������������KSCN��Ӧ�Ժ�ɫ��
�ο��𰸣���1��20.45%����3�֣�?��2��BaFe2O4(��BaO��Fe2O3)
�����������1�����������֪��4.66g���������ᱵ�����ʵ�����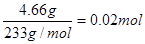
3.20 g�����������������ʵ�����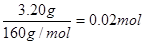
���12.52g��Ʒ����Ԫ�ص�������12.52g����0.02mol��137g/mol��0.02mol��2��56g/mol����2��2.56g
������ԭ�ӵ����ʵ�����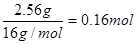
����Ԫ�ص�����������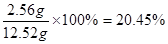
��2����Ʒ��Ba��Fe��Oԭ�ӵĸ���֮����0.02��2�U0.02��2��2�U0.16��1�U2�U4
���Ի�ѧʽΪBaFe2O4(��BaO��Fe2O3)��
�����Ѷȣ���
3��ѡ���� ��֪ij�Ͻ𣨽���ͭ��������ͭ���������ʵ���֮��Ϊy mol������Cu�����ʵ�������Ϊa������ȫ��Ͷ��50 mL b mol��L��1��������Һ�У�����ʹ���ַ�Ӧ������NO��Ψһ�Ļ�ԭ���������˵����ȷ���ǣ�?��
A��������û��ʣ�࣬��Ӧ��ת�Ƶĵ�����ĿΪ2y NA
B��������ȫ���ܽ⣬����Һ��һ������Fe3+
C������Һ�н�������ֻ��Fe3+��Cu2+ʱ����a��b�Ĺ�ϵΪ��b��80 y��1��a��3��
D��������ȫ���ܽ⣬�Ҳ���336 mL���壨��״��������b��0.3
�ο��𰸣�C
���������A��Fe���ܱ�����ΪFe3+��Ҳ���ܱ�����ΪFe2+�����Է�Ӧ��ת�Ƶĵ�����Ŀ��һ��Ϊ2y NA������B��������ȫ���ܽ�ʱ��Fe������Fe2+����ʽ���ڣ���һ�� Fe3+������C��HNO3�ͽ�����Ӧ���μӷ�Ӧ��HNO3һ����������������NO����һ���������������������Σ���n(Cu)=aymol��n(Fe)="(1-a)y" mol?�������Ե�HNO3Ϊ2n[Cu(NO3)2]+3n[Fe(NO3)3]="2aymol+3(1-a)y" mol=(3-ay)mol���ɵ����غ�ɵã����ɵ�NO�����ʵ�����������ԭ���������n(NO)=[2aymol+(3-ay)mol]/3=(3-ay)/3mol�����Բμӷ�Ӧ���� �� n(HNO3)=(4-4ay/3)mol����bX0.05��(4-4ay/3)mol����b��80y(1-a/3)����ȷ��D����b=0.3ʱ���μӷ�Ӧ��HNO3���Ϊ0.05LX0.3mol?L?1 =0.015mol��n(NO)="(336/22.4)X1000=0.015" mo����Ϊ�μӷ�Ӧ��HNO3���ʵ���Ӧ�ô���0.015mol��������n(HNO3)=0.015mol����Ȼ������������
�����Ѷȣ�һ��
4��ѡ���� ��AlCl3��MgCl2�Ļ����Һ�У���μ���NaOH��Һֱ�������������ϣ�����NaOH����������ó��������ʵ�����ʾ��ͼ���£�b��NaOH�����Ϊ1L���������ж���ȷ����
��?��
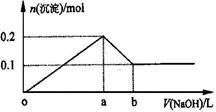
A�������Һ��Al3�������ʵ���Ϊ0.2mol
B��NaOH��Ũ��Ϊ0.5 mol/L
C����b�㴦��Һ�е�����ֻ��NaAlO2
D��ͼ���߶�oa : ab��5 : 1
�ο��𰸣�D
�����������Һ�з��� ��
�� ��
��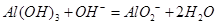 ��ͼ��֪��AlCl3��MgCl2�����ʵ�����Ϊ0.1mol����a������������ȫ������
��ͼ��֪��AlCl3��MgCl2�����ʵ�����Ϊ0.1mol����a������������ȫ������ ��ʼ�ܽ⣬��b��
��ʼ�ܽ⣬��b�� ��ȫ�ܽ⣬��Ϸ���ʽ���ɼ���õ�b��������0.6molNaOH
��ȫ�ܽ⣬��Ϸ���ʽ���ɼ���õ�b��������0.6molNaOH
A��Al3�������ʵ���Ϊ0.1mol��A�����
B��NaOH��Ũ��Ϊ0.6 mol/L��B�����
C����b�㴦��Һ�е�������NaAlO2��NaCl��C�����
D��ͼ��oa�����ĵ�NaOH�����ʵ���Ϊ0.5mol��ab�����ĵ�NaOH�����ʵ���Ϊ0.1mol�������߶�oa : ab��5 : 1��D����ȷ��
��ѡD
���������⿼�����Ρ�þ�����ķ�Ӧ�� ���Ժ�
���Ժ�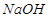 ��Ӧ����
��Ӧ����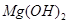 ���ܷ�Ӧ������Ӧ�������ʾ��ͼ�ͷ�Ӧ�ķ���ʽ�����
���ܷ�Ӧ������Ӧ�������ʾ��ͼ�ͷ�Ӧ�ķ���ʽ�����
�����Ѷȣ�һ��
5��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A��1molCl2������������Ӧ����FeCl3,ת�Ƶĵ�������3NA
B���ڱ�״���£�NA��ˮ������ռ�е����ԼΪ22.4L
C��7.8g Na2O2�к��������ӵ���ĿΪ0.1NA,������ˮ��Ӧʱ����ת����0.1NA
D��1mol�������е�ԭ������1mol�������е�ԭ����������
�ο��𰸣�CD
���������Aѡ����1molCl2������������Ӧ������ȫ�����ĸɾ�����Ԫ����ԭ����0��ȫ�����-1�ۣ���Ҫ�õ�������ĿΪ2NA������Ϊ��������ԭ��Ӧ�е�ʧ����Ҫ�غ㣬�����ܵ�ת�Ƶ�����ĿҲӦ����2NA��Bѡ����NA��ˮ�������ʵ���Ϊ1mol�����ڱ�״���£�ˮ�������壬���������Ӧ����22.4L��Cѡ���й����������������ǹ��������ӣ�7.8gNa2O2���ʵ���Ϊ0.1mol,��ô���������ӵ���ĿӦΪ0.1NA������ˮ��Ӧʱ�������Ʒ�������������ԭ��Ӧ�����������е�������ԭ��һ�����0�ۣ�һ����ɸ����ۣ�ת�Ƶ�����Ϊ0.1NA��Dѡ��������˫ԭ�ӷ��ӣ�1mol����ԭ����ĿΪ2NA��������Ϊ��ԭ�ӷ��ӣ�1mol�������е�ԭ������Ӧ��NA��
�����Ѷȣ�һ��