微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)在t℃时,某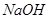 稀溶液中,
稀溶液中, ,
, ,已知
,已知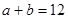 ,则:
,则:
(1)该温度下,水的离子积常数Kw=__________________。
(2)在该温度下,将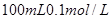 的稀硫酸与
的稀硫酸与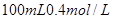 的
的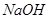 溶液混合后,溶液的pH=_________,此时该溶液中由水电离的
溶液混合后,溶液的pH=_________,此时该溶液中由水电离的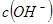 =_________。
=_________。
(3)该温度下,若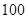 体积
体积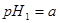 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的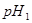 与强碱的
与强碱的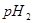 之间应满足的关系是_________。
之间应满足的关系是_________。
(4)该温度下, 的硫酸溶液和
的硫酸溶液和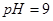 的
的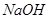 溶液等体积混合后,混合溶液的
溶液等体积混合后,混合溶液的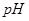 _________(填>7、=7、<7);
_________(填>7、=7、<7); 的醋酸溶液和
的醋酸溶液和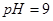 的
的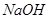 溶液等体积混合后,混合溶液的
溶液等体积混合后,混合溶液的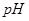 _________(填>7、=7、<7)。
_________(填>7、=7、<7)。
2、选择题 下列说正确的是
【已知:HClO的Ka=3.0×l0-8;H2CO3的Ka1= 4.3×l0-7,Ka2=5.6×l0-11;Ksp(BaSO4)=" 1.1" ×10-10;Ksp(BaCO3)=" 5.1" ×10-9】
A.相同条件下,pH相同的NaClO和Na2CO3溶液,物质的量浓度前者小于后者
B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7时:
c(Na+)>c(CH3COO-)>c(Cl-) >c(CH3COOH)>c(H+)=c(OH-)
C.向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小
D.氯碱工业使用的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂时,粗盐水中可先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后滤去沉淀,所得滤液中仍含有一定量的SO42-
3、填空题 常温下,有浓度均为0.1 mol/L的4种溶液:①盐酸;②硫酸;③醋酸;④氢氧化钡。(注:忽略溶液混合时 体积的变化)
(1)将上述溶液两两等体积混合后,溶液pH=7的组合有(填序号)_________。
(2)醋酸钡是易溶于水的强电解质。将③与④等体积混合,所得溶液中离子浓度由大到小的顺序是_____。
4、选择题 下列说法中,正确的是
A.常温下,某NaHSO3溶液的pH<7,则该溶液中c(SO32-)<c(H2SO3)
B.25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,所消耗溶液体积为:V(醋酸溶液)>V(NaOH溶液)
C.将l mL pH=2的醋酸溶液加水稀释到10 mL,pH变为3
D.常温下,将Na2CO3溶液加水稀释,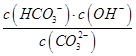 的值增大
的值增大