微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某一反应体系中共有Pb3O4、NO、MnO2、Cr2O3、Cr(MnO4)2和Pb(N3)2(名称叠氮化铅,其中Pb为+2价)六种物质,已知Pb(N3)2是反应物之一,Cr2O3是产物之一。请回答下列问题:
(1)已知Cr的常见化合价为+2、+3、+6,Mn的常见化合价为+2、+4、+6、+7,则Cr(MnO4)2中Cr的化合价为 ?。
(2)1mol Pb(N3)2在反应中 ?(填“得到”或“失去”)?mol电子。
(3)写出该反应的化学方程式?。
参考答案:(8分,每空2分)
(1)+2?(2)失去? 44/3或14.6
(3)15 Pb(N3)2+ 44Cr(MnO4)2=5Pb3O4+90NO↑+88MnO2+22Cr2O3
本题解析:Pb(N3)2是反应物之一,Pb3O4、NO肯定是产物,Pb(N3)2是不原剂,另一反应物中元素化合价要降低,Cr(MnO4)2是氧化剂,MnO2是还原产物。
(1)Cr(MnO4)2中Cr的化合价由化学式可知,肯定是偶数,由化合价代数和等于0,Mn为+7价时,Cr为+2价,合理;Mn为+6价时,Cr为+4价,不合理;答案:+2;⑵Pb(N3)2中Pb由+2价升高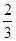 价,变成
价,变成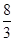 ,N由-
,N由-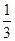 升高
升高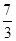 变成+2价,1mol Pb(N3)2在反应中共失去
变成+2价,1mol Pb(N3)2在反应中共失去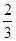 +6×
+6×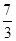 =
=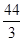 ,答案:失去? 44/3或14.6;⑶1mol Pb(N3)2在反应中共失去
,答案:失去? 44/3或14.6;⑶1mol Pb(N3)2在反应中共失去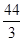 mol电子,1molCr(MnO4)2得到6mol电子,失去1mol电子,净得5mol电子,由得失电子守恒可配平方程式:Pb(N3)2前配15,Cr(MnO4)2前配44,再根据质量守恒,不难将方程式配平,15 Pb(N3)2+ 44Cr(MnO4)2=5Pb3O4+90NO↑+88MnO2+22Cr2O3,答案:15 Pb(N3)2+ 44Cr(MnO4)2=5Pb3O4+90NO↑+88MnO2+22Cr2O3。
mol电子,1molCr(MnO4)2得到6mol电子,失去1mol电子,净得5mol电子,由得失电子守恒可配平方程式:Pb(N3)2前配15,Cr(MnO4)2前配44,再根据质量守恒,不难将方程式配平,15 Pb(N3)2+ 44Cr(MnO4)2=5Pb3O4+90NO↑+88MnO2+22Cr2O3,答案:15 Pb(N3)2+ 44Cr(MnO4)2=5Pb3O4+90NO↑+88MnO2+22Cr2O3。
本题难度:一般
2、选择题 在反应2KClO3="==2KCl" + 3O2↑中,电子转移的总数是(?)
A.2个
B.6个
C.12个
D.5个
参考答案:C
本题解析:在反应2KClO3="==2KCl" + 3O2↑中KClO3中的Cl是+5价,KCl中的Cl是-1价,KClO3→KCl转移的是6个电子,2KClO3→2KCl是12个电子。
点评:解决此类题目的关键是掌握氧化还原反应的基本概念,部分元素化合价发生变化的反应要看清楚发生化合价变化的原子个数。
本题难度:简单
3、选择题 人体不能够吸收+3价的铁元素,能够吸收的是+2价的铁元素,而天然食品中所含的铁元素大多是+3价的,为了将天然食品中的Fe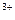 转化为Fe
转化为Fe ,可加入维生素C(VC)。下列关于维生素C的说法正确的是(?)
,可加入维生素C(VC)。下列关于维生素C的说法正确的是(?)
A.VC的氧化性比Fe 的强
的强
B.VC的还原性比Fe 的强
的强
C.VC的还原性比Fe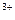 的强
的强
D.VC的氧化性比Fe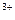 的强
的强
参考答案:B
本题解析:该变化过程(Fe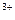 →Fe
→Fe )属于还原反应,应该选择还原剂,且所选还原剂的还原性必须强于还原产物Fe
)属于还原反应,应该选择还原剂,且所选还原剂的还原性必须强于还原产物Fe 的还原性。
的还原性。
本题难度:一般
4、填空题 已知硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。
(1)请写出并配平上述反应的化学方程式:?。
(2)此反应的还原剂是___________,它的氧化产物是?。
(3)此反应的离子反应方程式可表示为:________________________________________。
(4)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有___________。
参考答案:(1)2MnSO4+5K2S2O8+8H2O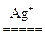 2KMnO4+4K2SO4+8H2SO4
2KMnO4+4K2SO4+8H2SO4
(2)MnSO4? KMnO4
(3)2Mn2++5S2O +8H2O
+8H2O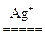 2MnO
2MnO +10SO
+10SO +16H+
+16H+
(4)Cl2(答HClO或HClO3也给分)
本题解析:此题考查了氧化还原方程式的配平及氧化还原反应的基本概念。在反应过程中MnSO4中的Mn元素由+2价被氧化为+7价生成MnO ,故MnSO4为还原剂,其氧化产物为KMnO4。如把MnSO4改为MnCl2,因Mn2+的还原性比Cl-弱,K2S2O8首先氧化Cl-生成Cl2,过量的K2S2O4再氧化Mn2+生成KMnO4。
,故MnSO4为还原剂,其氧化产物为KMnO4。如把MnSO4改为MnCl2,因Mn2+的还原性比Cl-弱,K2S2O8首先氧化Cl-生成Cl2,过量的K2S2O4再氧化Mn2+生成KMnO4。
本题难度:简单
5、选择题 工业上生产MnO2和Zn的主要反应有:
①MnO2+ZnS+2H2SO4==MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
MnO2+Zn+2H2SO4
下列说法不正确的是
[? ]
A.①中MnO2和H2SO4都是氧化剂
B.①中析出16gS时转移lmol电子
C.②中MnSO4发生氧化反应
D.硫酸在该生产中可循环利用
参考答案:A
本题解析:
本题难度:简单