微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。

(1)写出反应①的化学方程式:?。
(2)反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂?。
(3)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有?。
(4)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式为?。
(5)工业上制备还原性气体CO和H2的反应原理为CO2+CH4 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为?。
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为?。
参考答案:(1)2MoS2+7O2 2MoO3+4SO2
2MoO3+4SO2
(2)H2SO4、Na2SO3[或Na2SO4、(NH4)2SO4等]
(3)烧杯、漏斗、玻璃棒
(4)Na2MoO4
(5)4.11a g
本题解析:(1)二硫化钼与氧气在高温下反应生成三氧化钼和二氧化硫。
(2)二氧化硫可收集再利用,制备硫酸和盐类等。
(3)操作1和操作2都是分离固体与液体混合物,都是过滤操作。
(4)钼酸是二元酸,可直接写出钼酸钠。
(5)根据反应方程式知,1 mol甲烷完全反应生成4 mol还原性气体,而:3CO+MoO3 Mo+3CO2,3H2+MoO3
Mo+3CO2,3H2+MoO3 Mo+3H2O,3 mol还原性气体理论上生成1 mol钼。n(CH4)=
Mo+3H2O,3 mol还原性气体理论上生成1 mol钼。n(CH4)=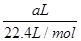 ×80%,n(H2+CO)=
×80%,n(H2+CO)=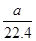 ×80%×90%×4 mol=
×80%×90%×4 mol=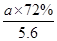 ,n(Mo)=
,n(Mo)=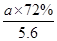 ×
×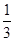 mol=
mol=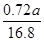 ?mol,m(Mo)=
?mol,m(Mo)=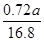 mol×96 g・mol-1≈4.11a g。
mol×96 g・mol-1≈4.11a g。
本题难度:一般
2、填空题 483g?Na2SO4?10H2O中所含的Na2SO4?10H2O的物质的量是______,Na2SO4?10H2O的摩尔质量是______所含SO42-的物质的量是______,所含Na+的物质的量是______?所含H2O分子的数目是______个.
参考答案:M(Na2SO4?10H2O)=322g/mol,n(Na2SO4?10H2O)=483g322g/mol=1.5mol,
n(SO42-)=n(Na2SO4?10H2O)=1.5mol,
n(Na+)=2n(Na2SO4?10H2O)=2×1.5mol=3mol,
n(H2O)=10n(Na2SO4?10H2O)=10×1.5mol=15mol,
N(H2O)=15mol×NA个/mol=15NA(或9.03×1024),
故答案为:1.5mol;322g/mol;1.5mol;3mol;15NA(或9.03×1024).
本题解析:
本题难度:一般
3、填空题 某气体的摩尔质量是Mg/mol,分子数为x,在标准状况下所占的体积是VL,质量是mg。某元素原子的摩尔质量是Ag/mol,原子个数是Y,阿伏加德罗常数为NA。 试说明下列各式表示的意义。
?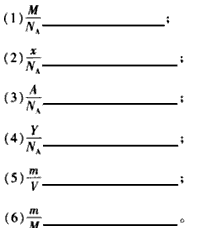
参考答案:(1)该气体一个分子的质量
(2)该气体的物质的量
(3)该元素一个原子的质量
(4)该元素原子的物质的量
(5)标准状况下该气体的密度
(6)该气体的物质的量
本题解析:
本题难度:一般
4、选择题 配制450毫升1mol/L的食盐溶液需选择的容量瓶是(?)
A 100ml? B 500ml? C 450ml? D50ml
参考答案:B
本题解析:
正确答案:B
没有450毫升规格的容量瓶,一次配成450毫升溶液,只能选500毫升的容量瓶
本题难度:简单
5、选择题 质量分数为15%的硫酸溶液18 mL,密度为1.102 g・m-1,则它的物质的量浓度最接近下列数值中的(?)
A.1.685 mol・L-1
B.3.370 mol・L-1
C.22.49 mol・L-1
D.11.24 mol・L-1
参考答案:A
本题解析:由于题中给出的各选项之间的数值相差都比较大,所以可以进行近似处理:1.102→1,98→100,代入公式c= =1.5,与A选项较接近。
=1.5,与A选项较接近。
本题难度:简单