微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NA?表示阿伏加德罗常数,下列叙述中,正确的是( )
A.1molH2?所含的中子数是2NA
B.4℃时,3.6mLH2O?所含水分子为0.3NA
C.24g氮气所含的原子数为NA
D.1molNa作还原剂可提供的电子数为NA
2、实验题 (17分)科学探究
某学习小组根据图中所示的电解水原理进行实验,并对实验得到的与查阅资料获得的数据进行处理、分析,请与他们一起进行探究。请按要求填写。
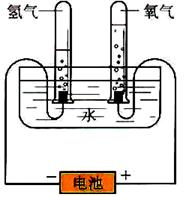
(1)观察不同时间试管内的H2和O2体积的比值均约为 。
(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成H2、O2的质量,计算过程如下:
并填表如下:
| 质量g
| 物质的量mol
| H2和O2物质的量的比
|
H2
|
|
|
|
O2
|
|
|
根据该实验的观察与推算初步得到关于气体体积规律的一个结论是:在相同的温度和压强下,
(3)下表列出了一些物质的体积
条件
| 物质
| 1 mol物质的体积
|
0℃101kPa
| H2
| 22.3 L
|
O2
| 22.4 L
|
CO2
| 22.4 L
|
25℃101kPa
| H2
| 24.4L
|
O2
| 24.5L
|
CO2
| 24.5L
|
根据上表数据,得出的结论是(至少写出三点)
①在相同的温度压强下,
②
③
④
(4)请从微观的角度解释气体体积变化规律的原因:
3、选择题 若NA代表阿伏加德罗常数,则下列叙述中,正确的是
[? ]
A.?一定条件下,足量铜与200?g?98%的浓硫酸充分反应,转移电子数目为2NA
B.?t℃时,1LpH=6的纯水中,含10-6NA个OH-?
C.?1mol?FeCl3溶于水转化为氢氧化铁胶体后,其中氯离子的数目小于3NA?
D.?标准状况下,一定量的铜与硝酸反应后生成22.4?L?NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数为NA
4、选择题 阿伏加德罗常数的单位是
[? ]
A.NA
B.mol
C.mol-1
D.没有单位
5、选择题 设NA为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,224?mL水含有的电子数为0.1NA
B.1L?0.1mol/L硅酸钠溶液中含有0.1NA个SiO2-3
C.标准状况下,11.2?LCO2和SO2混合气体中含NA个氧原子
D.足量的铁粉与1mol?Cl2加热条件下充分反应,转移的电子数为3NA