微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组离子在指定溶液中,能大量共存的是?(?)
A.强碱性溶液中:K+,ClO-,Ba2+,Cl-
B.水电离的H+浓度c(H+)=10-12mol・L-1的溶液中:Cl-,CO32-,NO3-,NH4+
C.使甲基橙变红的溶液中:Fe2+,MnO4-,NO3-,Na+
D.中性溶液中:Al3+,NO3-,Cl-,S2-
参考答案:A
本题解析:略
本题难度:一般
2、选择题 下列各组离子在指定溶液中,一定能大量共存的是?
A.常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+
B.中性溶液:Fe3+、Al3+、NO3-、SO42-
C.加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-
D.常温下由水电离出的c(H+)=10-10mol・L-1的溶液:Na+、Cl-、ClO-、SO32-
参考答案:A
本题解析:A:溶液呈强碱性,各离子可大量共存
B:Fe3+在pH>3时即可完全水解为沉淀,故排除
C:加入苯酚显紫色的溶液,也就是含有FeCl3溶液,I-可被其氧化,排除
D:ClO-、SO32-分别具有强氧化性和还原性,可发生氧化还原反应,不能大量共存,排除
本题难度:一般
3、选择题 下列各组离子在溶液中可以大量共存的是
A.H+、SO32-、S2-、K+
B.Fe3+、Cl-、S2-、Ba2+
C.Cu2+、Cl-、S2-、K+
D.Na+、K+、S2-、SO42-
参考答案:D
本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A中H+、SO32-、S2-三者发生氧化还原反应生成单质S沉淀;B中Fe3+能氧化S2-不能大量共存;C中Cu2+和S2-反应生成CuS沉淀,不能大量共存,所以正确的答案选D。
点评:该题是高考中的高频题,属于中等难度的试题,侧重对学生基础知识的训练和检验。有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题需要明确离子不能大量共存的一般情况,即(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(4)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”。
本题难度:一般
4、选择题 室温时,下列各组离子在指定溶液中可以大量共存的是
A.由水电离出的c(H+)=10-12mol/L的溶液中:Na+、Ba2+、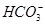 、Cl-
、Cl-
B.无色透明溶液中:K+、Cu2+、SO42-、Na+
C.含有大量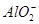 的溶液中:Na+、OH-、Cl-、
的溶液中:Na+、OH-、Cl-、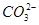
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、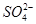
参考答案:C
本题解析:A项,该溶液呈酸性或碱性,无论该溶液呈酸性还是呈碱性,碳酸氢根离子都不能大量共存。B项,铜离子呈蓝色。D项,使pH试纸显红色的溶液显酸性,酸性条件下,次氯酸根离子有强氧化性,能氧化二价铁离子,所以不能共存。
本题难度:一般
5、选择题 某碱性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是(? )
A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.在NaOH溶液中加入一定量的CH3COOH溶液,只有当溶液中离子浓度满足:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,才符合题意。
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
参考答案:B
本题解析:首先要强调隐含条件“碱性”,得出:c(OH-)>c(H+),再根据电荷守恒推出(Na+)>c(CH3COO-)。
A项恰好满足n(OH-)=n(H+),即酸和碱已电离出来的、H+、OH-恰好完全中和,但是由于醋酸是弱酸,大量的未电离,即大量剩余,故混合后溶液呈酸性。
B项是等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合,则恰好中和转化成为CH3COONa溶液,属于强碱弱酸盐溶液,故呈碱性,合乎题意。
C项中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,是满足题意的唯一条件吗?这是本题的难点,实际上c(Na+)>c(OH-)>c(CH3COO-)>c(H+)也可以,相当于加入的醋酸很少。
D项是在原溶液中加入适量氨水,溶液仍呈碱性,根据c(OH-)>c(H+)、(Na+)>c(CH3COO-),得出c(CH3COO-)一定大于c(Na+)、c(NH4+)之和的说法是错误的。
本题难度:简单