��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����β���ﺬ���ж���NO��CO��NO��CO�ܻ����ط�Ӧ����N2��CO2���Դ˷�Ӧ��������������ȷ���ǣ�������
A��ʹ�ô����ܼӿ췴Ӧ����
B�������¶��ܼӿ췴Ӧ����
C���ı�ѹǿ�Է�Ӧ������Ӱ��
D���˷�Ӧ�ܼ���β���Ի�������Ⱦ
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� ��X��Y��Z�Ƕ�����Ԫ�ص����ֳ��������X��ˮ��Ӧ������һ�־��л�ԭ�ԵIJ��ȶ��Ķ�Ԫ�ᣬ����Ļ�ѧʽ��______��Y��X���Ԫ����ͬ��Y��ˮ��Ӧ����M������M��Ũ��Һ��3.2g?Cu�ڼ��������³�ַ�Ӧ�����б���ԭ��M�����ʵ���Ϊ______����̬Z��Ӧ�����˹����꣬0.5mol?L-1Z��NaOH��Ӧ���õ�����ˮ��Һ�У�����Ũ�ȴӴ�С��˳��Ϊ______��
��N2O5��һ�������������������ʺ��Ʊ��ܵ����ǵĹ�ע������H2��O2��������Na2CO3��ɵ�ȼ�ϵ�أ�����YΪCO2�����õ�ⷨ�Ʊ�N2O5���ܵķ�Ӧ����ʽΪ��N2O4+2HNO3=2N2O5+H2��װ����ͼ��ʾ��
д��ʯīI�缫�Ϸ�����Ӧ�ĵ缫��Ӧʽ______��
�ڵ���������N2O5�ĵ缫��ӦʽΪ______��
������������SO2����������������NOx���������ǻ�����ѧ�о����ȵ㣮
��1���������������Ի���������______��
��2��Ŀǰ����ѧ�������о�һ������ϩ��Ϊ��ԭ����������NO��ԭ��������������ʾ��ͼ��ͼ1��
���������¶ȡ������ʣ�����ɸ�д����������������Ĺ�ϵ��ͼ2��ʾ��
��д��������ԭ���ܷ�Ӧ�Ļ�ѧ����ʽ��______����Ϊ�ﵽ�������Ч����Ӧ��ȡ��������______��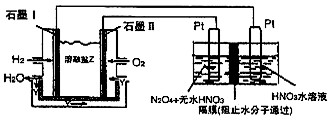
�ο��𰸣������Ķ�Ԫ��������H2SO4��H2SO3��H2CO3��H2SiO3�����л�ԭ�ԵĶ�Ԫ������Ϊ�����ᣬ��ѧʽ��H2SO3������XΪ��������
Y��X���Ԫ����ͬ������Y����������M�����ᣬŨ�����ͭ��Ӧ�ķ���ʽΪ
Cu+H2SO4��Ũ��+H2SO4��Ũ�� ������ԭ���ᣩ?��?.?CuSO4+SO2��+2H2O��
64g? 1mol
3.2g?0.05mol
���Ա���ԭ������Ϊ0.05mol��
��̬��Ӧ�����˹������������Ϊ������̼������Z�Ƕ�����̼��������̼��NaOH��Ӧ���õ�����Ϊ̼���ƣ�̼������ǿ�������Σ������ܵ���Ҳ��ˮ�⣬ֻ�ǵ���̶ȴ���ˮ��̶ȣ�����̼�������Ũ�ȴ���̼���������Ũ�ȣ�̼���Ƕ�Ԫ���ᣬ����̼��������ܷ�������ˮ�⣬��һ��ˮ��̶ȴ��ڵڶ���ˮ��̶ȣ�̼�������ÿ�������������������ɣ��������������ӵ�Ũ�ȴ���̼��������ӵ�Ũ�ȣ�̼������ǿ�������Σ���ˮ��Һ�ʼ��ԣ���������������Ũ�ȴ���������Ũ�ȣ�������Һ�����ӵ�Ũ�ȴ�СΪC��Na+����C��CO32- ����C��OH-����C��HCO3-����C��H+����
�ʴ�Ϊ��H2SO3��0.05mol��C��Na+����C��CO32- ����C��OH-����C��HCO3-����C��H+����
��ȼ��ԭ����У�������ȼ��ʧ���Ӻ�̼������ӷ�Ӧ���ɶ�����̼��ˮ���缫��ӦʽΪH2+CO32--2e-=CO2+H2O��
N2O5�е�Ԫ�صĻ��ϼ���+5�ۣ��������е�Ԫ��Ҳ��+5�ۣ����Ӧ�����������N2O5�����������������ɣ��ݵ缫��Ӧ���ӷŵ�˳���֪����������2H++2e-=H2���ķ�Ӧ��������ΪN2O4+2HNO3-2e-=2N2O5+2H+��
�ʴ�Ϊ��H2+CO32--2e-=CO2+H2O��N2O4+2HNO3-2e-=2N2O5+2H+��
��1����SO2�͵��������NOx���������������Ҫ���ʣ������������������Ļ��������Ƿ�ֹ���ꡢ�⻯ѧ�����ķ������ʴ�Ϊ����ֹ���ꡢ�⻯ѧ�����ķ�����
��2������ͼ1֪����Ӧ��Ϊһ����������������ϩ��ͭΪ������������Ϊ������������̼��ˮ����Ӧ����ʽΪ6NO+3O2+2C2H4?����?.?3N2+4CO2+4H2O��
�ʴ�Ϊ��6NO+3O2+2C2H4?����?.?3N2+4CO2+4H2O����
�����������ʸߣ������ʵͣ����˵��¶ȣ���ͼ��֪���ʺ�����Ϊ350�桢������3%���ʴ�Ϊ��350�桢������3%��
���������
�����Ѷȣ�һ��
3��ѡ���� ͬ��ͬѹ�£�����������ĸ�����ƿ�зֱ������NH3����NO2��������Ȫʵ�飬��ͼ��ʾ������ַ�Ӧ��ƿ����Һ�����ʵ���Ũ��
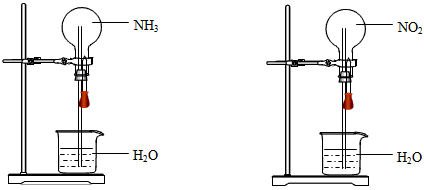
[? ]
A����>��
B����<��
C����=��
D������ȷ��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ��ʢ��amolNO2��bmolNO����״���£����������Թܵ���������ʢ��ˮ��ˮ���У���ͨ��bmolO2����ַ�Ӧ���Թ���ʣ�������ijɷּ����ʵ���ȡ����a��b�Ĺ�ϵ���������ж���ȷ���ǣ�������
������NO����a��b����ʣ����������ʵ���Ϊ
������O2����a��b����ʣ����������ʵ���Ϊ
����������ʣ�࣬��a=b����������Һ�����ʵ���Ũ��Ϊmol��L-1��
A��ֻ�Т���ȷ
B��ֻ�Т���ȷ
C���٢ڢ۶�����ȷ
D���٢ڢ۶���ȷ
�ο��𰸣�������NO�������������
��ֻ������Ӧ4NO2+O2+2H2O=4HNO3����4bmol=amol����a=4b��NOδ��Ӧ��ʣ��NOΪbmol��
������Ӧ4NO2+O2+2H2O=4HNO3��3NO2+H2O=2HNO3+NO����4bmol��amol����a��4b����ˮ��Ӧ��NO2Ϊ��a-4b��mol
ʣ��NOΪbmol+13��a-4b��mol=13��a-b��mol��
������Ӧ4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O�T4HNO3����NO2��Ҫ������Ϊ14amol����NO��Ӧ������Ϊbmol-14amol��NO��ȫ��Ӧ��Ҫ����Ϊ34bmol������NOʣ�࣬��34bmol��bmol-14amol������a��b��
��b-14a��mol������Ӧ��NOΪ43��b-14a��mol����ʣ��NOΪbmol-43��b-14a��mol=13��a-b��mol��
�ʢٴ���
�ڡ�����O2������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O�T4HNO3����NO2��NO��ȫ��Ӧ����NO2��Ҫ������Ϊ14amol��NO��Ҫ����Ϊ34bmol����Ϊ14amol+34bmol��bmol��������a��b��ʣ������Ϊbmol-��14amol+34bmol��=14��b-a��mol���ʢ���ȷ
��
�ۡ���������ʣ�࣬����4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O�T4HNO3����NO2��Ҫ������Ϊ14amol��NO��Ҫ����Ϊ34bmol
��Ϊ14amol+34bmol=bmol��������a=b������NԪ���غ�n��HNO3��=n��NO��+n��NO2��=��a+b��mol����Һ�������NO��NO2�����֮��Ϊ��a+b��mol��22.4L/mol=22.4��a+b���������Ũ��Ϊ(a+b)mol22.4(a+b)L=122.4mol/L���ʢ۴���
��ѡB��
���������
�����Ѷȣ�һ��
5��ѡ���� ���䡰�����������ػ�������ƽ�����ȼ�������ҷ�Ӧ����������������ɫ���壨CO2��H2O��N2��NO���ӻ��β����������ڷ����ֳ��������β����������غ�ɫ�����壬�����غ�ɫ�������ԭ���ǣ�������
A��NO����������NO2
B��������N2����������NO2
C��CO2��N2��Ӧ����CO��NO2
D��NO��H2O��Ӧ����H2��NO2
�ο��𰸣�A
���������
�����Ѷȣ�һ��