| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《无机综合与推断》高频试题特训(2017年最新版)(二)
(3)由溶液C获得CuSO4・5H2O,需要经过?,过滤等操作。除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是?。 (4)制备CaCO3时,先通入?(填NH3或CO2),若实验过程中有氨气逸出,可选用下列装置中的? ?(填代号)装置吸收氨气。(烧杯中的液体都为水) 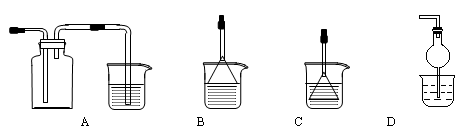 参考答案:(1)SiO2 (1分)?, D(1分) 本题解析:(1)SiO2不溶于硫酸;Fe3+遇 KSCN溶液变成血红色,是Fe3+的特性,不会受到其他离子的干扰。(2)加入双氧水使二价铁离子转变为三价铁离子,最后以氢氧化铁形式析出;除去杂质的原则是不引入新的杂质。(3)溶液析出固体的实验操作。(4)制备CaCO3时会吸收气体,为防止倒吸,选用BC装置。 本题难度:一般 4、填空题 (10分)A、B、C、D和甲有以下转化关系。已知物质甲是短周期元素组成的盐,且是某 参考答案:(10分) (1)四? VIII 本题解析:略 本题难度:简单 5、填空题 (10分)A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。 参考答案: 本题解析:略 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《电解质溶液.. | |