微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (15分)Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物。
[实验步骤]
I、按下图所示装置(部分仪器未画出)组装仪器,并检查装置气密性。
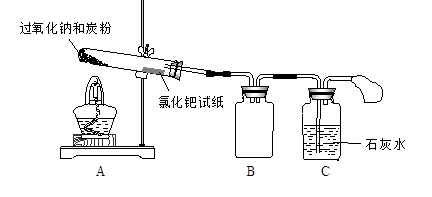
 II. 将0.6 g炭粉与3.9 g Na2O2均匀混合,装入试管,在靠近试管口处放置一张湿润的
II. 将0.6 g炭粉与3.9 g Na2O2均匀混合,装入试管,在靠近试管口处放置一张湿润的
氯化钯试纸(湿润氯化钯试纸遇CO变黑,可用于检验是否有CO生成)。
III. 用酒精灯微微加热试管底部。
[实验现象]
试管中发生剧烈反应并产生火花,氯化钯试纸未变黑,石灰水未变浑浊。
请回答:
(1)装置B的作用是?。
(2)通过探究发现,装置A中只发生反应2Na2O2+C Na2CO3+X,则X为?(填化学式),①请设计实验证明产物X的存在,简要写出操作方法、现象和结论:
Na2CO3+X,则X为?(填化学式),①请设计实验证明产物X的存在,简要写出操作方法、现象和结论:
??。
②有人认为炭粉的加入量的多少会影响产物X的检验,请简要说明原因:
?
(3)CO在潮湿环境中可将氯化钯还原为黑色粉末状的钯(Pd:Mr=106),同时生成另外两种新物质。已知反应过程中转移6.02×1023个电子时,生成53 g Pd,该反应的化学方程式为?。
(4)将装置A中完全反应后所得物质溶于适量水,配成溶液,回答下列问题:
①溶液中下列关系正确的是?(填字母序号)。
a.c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)?
b.c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)
c.c(Na+)=2[c(CO32-)+c(HCO3-)+ c(H2CO3)]?
d.c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-)
②若使所得溶液与100 mL稀盐酸恰好完全反应至溶液pH=7,该盐酸的物质的量浓度为?。
参考答案:(1)防止倒吸? (2分)?(2)? Na2O? (2分)
①将产物溶于水,加入足量的BaCl2溶液,若有白色沉淀生成,则有Na2CO3; 再滴加酚酞,溶液变红,说明有Na2O 。?(其他合理答案均可) ?(3分)
②假如加入C的量不足,过量的过氧化钠与水反应生成碱,使酚酞溶液变红。?(2分)
(3)PdCl2 + CO + H2O ="==" Pd + CO2 + 2HCl? (2分)
(4)① b d(少选得1分,多选、错选0分)?(2分)
②? 1 mol/L?(漏写单位不给分)?(2分)
本题解析:(1)CO2溶于澄清石灰水中有可能倒流,所以装置B的作用是防止倒吸。
(2)根据原子守恒可知,X应该是氧化钠。
①氧化钠溶于水生成氢氧化钠,显碱性,据此可以鉴别。由于碳酸钠溶于水也显碱性,所以需要先除去碳酸钠,所以正确的方法是将产物溶于水,加入足量的BaCl2溶液,若有白色沉淀生成,则有Na2CO3; 再滴加酚酞,溶液变红,说明有Na2O 。
②如果碳不足,则过氧化钠过量,而过氧化钠溶于水也产生氢氧化钠,会干扰氧化钠的检验。
(3)53 g Pd是0.5mol,反应中转移电子是1mol,所以氧化产物是CO2,则方程式为PdCl2 + CO + H2O ="==" Pd + CO2 + 2HCl。
(4)①所得产物是碳酸钠和氧化钠,溶于水生成氢氧化钠。由于碳酸钠水解,所以选项a不正确,b正确。由于氢氧化钠和碳酸钠的物质的量相等,所以c不正确。d符合电荷守恒,正确。答案选bd。
②过氧化钠是3.9g÷78g/mol=0.05mol,根据钠原子守恒可知,氯化钠是0.1mol,所以浓度是0.1mol÷0.1L=1.0mol/L。
本题难度:一般
2、实验题 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
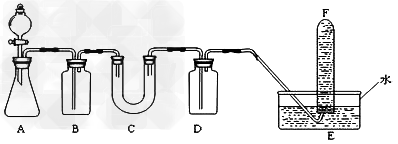
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:______________________。
(2)填写表中空格。
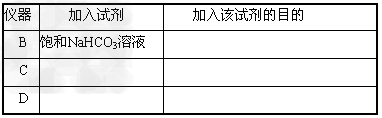
(3)写出过氧化钠与二氧化碳反应的化学方程式:_______________________。
(4)试管F中收集满气体后,下一步实验操作是:_______________________。
参考答案:(1)CaCO3+2HCl?=?CaCl2?+?H2O?+?CO2↑?
(2)除去CO2中混入的HCl;过氧化钠;与CO2和水蒸气反应,产生O2;NaOH溶液;吸收未反应的CO2气体?
(3)2Na2O2+2CO2=2NaCO3+O2?
(4)把E中导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即将带火星的木条伸入试管口内,若带火星的木条复燃,则证明试管中收集的气体是O2
本题解析:
本题难度:一般
3、填空题 (12分)根据要求填写:
(1)金属钠在空气中燃烧,火焰呈?色,化学方程式:?;
(2)将过氧化钠固体放入试管中加入少量水,再加入几滴酚酞试液,溶液变红色但很快褪色,原因是:?,过氧化钠固体与水反应的化学方程式:? ?;
?;
(3)苏打和小苏打分别和同浓度的盐酸反应,反应较快且剧烈的是?(填化学式),小苏打与盐酸反应的离子方程式为:? ?;
?;
(4)金属钠和金属钾分别和水反应试验中,其中反应较剧烈的反应的化学方程式:?;
参考答案:(12分)
(1)黄(1分),2Na+O 2====Na2O2(2分)
2====Na2O2(2分)
(2)过氧化钠有强氧化性(或过氧化钠有漂白性)(2分),2Na2O2+2H2O=4NaOH+O 2↑(2分)
2↑(2分)
(3)NaHCO3(1分),HCO3―+ H+= H2O+CO2↑(2分)
H+= H2O+CO2↑(2分)
(4)2K+2H2O=2KOH+H2↑(2分)
本题解析:略
本题难度:一般
4、计算题 200 ℃时,11.6 g CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体质量增加了3.6 g。求混合物中CO2和H2O的质量比。
参考答案:设混合物中CO2和H2O的质量分别为x、y。
2CO2+2Na2O2====2Na2CO3+O2Δm
88 56
x?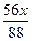
2H2O+2Na2O2====4NaOH+O2↑ Δm
36? 4
y?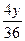
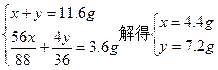
故:m(CO2)∶m(H2O)=4.4∶7.2=11∶18。
混合物中CO2和H2O的质量比为11∶18。
本题解析:本题可用“差量法”解题,设未知数,列方程组求解。
本题难度:简单
5、选择题 某烧碱溶液部分变质生成了少量纯碱,要除去此杂质需加适量的(?)
A.CaCl2溶液
B.Ca(OH)2
C.BaCl2
D.CO2
参考答案:B
本题解析:除杂的原则之一:不能引入新杂质。A、C选项均引入Cl-,D选项中CO2,还能与NaOH反应。
本题难度:简单