��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ִ���ҵ��ú̿�������ȿ������ȼ�ϵ������ʡ�����CO��SO2�ȵ��ŷţ��ֿ�������ˮú���Ĺ㷺��;��
����֪��2C(s)+O2(g)��2CO(g)����H1 ,? 2H2(g)+O2(g)��2H2O(g)����H2 ��
��ӦC(s)+H2O(g)  CO(g)+H2(g)����H��?��?�����ú���H1����H2�Ĵ���ʽ��ʾ��
CO(g)+H2(g)����H��?��?�����ú���H1����H2�Ĵ���ʽ��ʾ��
��CO��H2��һ�������ºϳɼ״��ķ�ӦΪ��CO(g)+2H2(g)  CH3OH��g������H3�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1mol?CO��2mol?H2�Ļ�����壬���£�����ʵ�飬��������������ͼ1��ͼ2��
CH3OH��g������H3�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1mol?CO��2mol?H2�Ļ�����壬���£�����ʵ�飬��������������ͼ1��ͼ2��
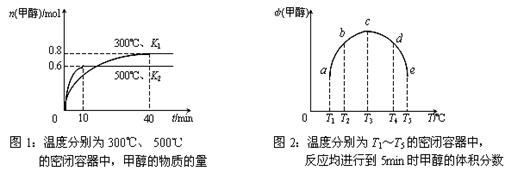
�ٸ÷�Ӧ�Ħ�H3??�� ?0��ѡ���������������=������ͬ����K1?��?K2��
�ڽ�����c�е�ƽ��״̬ת�䵽����d�е�ƽ��״̬���ɲ�ȡ�Ĵ�ʩ��?��?��
��ijȼ�ϵ����COΪȼ�ϣ��Կ���Ϊ��������������̬K2CO3Ϊ����ʡ�д����ȼ�ϵ�ظ����ĵ缫��Ӧʽ��?��?��
�ο��𰸣���(��H1����H2)/2
�Ƣ٣�����
�����»��ѹ
��CO��CO32����2e����2CO2
�����������
�����Ѷȣ�һ��
2������� ��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g) 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
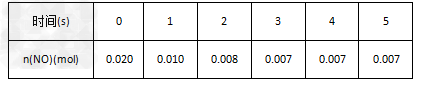
��1��NO��ƽ��Ũ��c(NO)=?��
��2����O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ����Ӧ����v= ? ��
��3����ͼ�б�ʾNO2�仯��������? ��
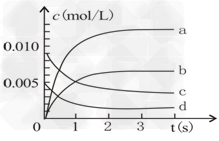
��4��800��ʱ����������ʼѹǿ��ƽ���ѹǿ֮��Ϊ___________________��
�ο��𰸣���1��3.5��10-3mol��L��1 ?
��2��1.5��10-3mol��L��1��s��1
��3��b ?
��4��3��2.35
���������
�����Ѷȣ�һ��
3������� (8��)���з�ӦaA(g)��bB(g)  pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����
pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����
(1)�÷�Ӧ������Ӧ��________�ȷ�Ӧ����a��b________p(�>����<������)��
(2)��ѹʱ��A����������________(�������С�����䡱����ͬ)������Ӧ����________��
(3)������B(�������)����A��ת����________��B��ת����________��
(4)�������¶ȣ���ƽ��ʱ��B��C��Ũ��֮��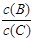 ��________��
��________��
(5)�����������ƽ��ʱ��������������ʵ���________��
�ο��𰸣�(1)����>��(2)����С��(3)����С��(4)��С��(5)����
�����������1�������¶�ʱ��B��ת���ʱ��˵�������¶ȣ�ƽ��������Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ����Сѹǿʱ�������ϵ��C������������С��˵������ѹǿ��ƽ�����淴Ӧ�����ƶ���������Ӧ�������С�ģ���a����p��
��2������ѹǿ��ƽ�����淴Ӧ�����ƶ�������A��������������Ӧ���ʶ��Ǽ�С�ġ�
��3������B��Ũ�ȣ�ƽ��������Ӧ�����ƶ�������A��ת��������B��ת���ʽ��͡�
��4�������¶ȣ�ƽ��������Ӧ�����ƶ�����C��Ũ������B��Ũ�ȼ�С����� ��С��
����
��5���������ܸı�ƽ��״̬������ƽ��ʱ��������������ʵ������䡣
�����Ѷȣ�һ��
4��ѡ���� ��4 mol A��2 mol B����2 L�ܱ������з�����Ӧ2A(g) + B(g) 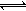 ?2C(g) ��H��0��4 s��Ӧ�ﵽƽ��״̬����ʱ���C��Ũ��Ϊ0.6 mol/L������˵����ȷ����
?2C(g) ��H��0��4 s��Ӧ�ﵽƽ��״̬����ʱ���C��Ũ��Ϊ0.6 mol/L������˵����ȷ����
A����c(A)�Uc(B)�Uc(C)��2�U1�U2ʱ���÷�Ӧ���ﵽƽ��״̬
B���ﵽƽ��״̬�����¶Ȳ��䣬��С�������������A��ת���ʽ���
C���ﵽƽ��״̬����ֻ�����¶ȣ���C�����ʵ���Ũ������
D��4 s�ڣ�v(B)��0.075 mol/(L ��s)
�ο��𰸣�D
���������A����÷�Ӧ����������Ũ��֮�ȵ��ڼ���ϵ��֮�����жϴ�ƽ�⡣B����С�����������ѹǿ����ƽ�������ƶ���A��ת�������ߡ�C�������¶ȣ�ƽ�������ƶ���C��Ũ�Ƚ�С��D��4s�ڣ�v(C)=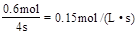 ����v(B)= 0.075 mol/(L ��s)����ѡD��
����v(B)= 0.075 mol/(L ��s)����ѡD��
�������жϻ�ѧƽ��״̬�ı�־�У�(1)�κ�����¾�����Ϊ��־�ģ��٦���=����(ͬһ������)���ڸ���ֺ���(�ٷֺ��������ʵ���������)����ʱ��仯����ij��Ӧ�������(����)���ʡ�ij�����������(����)����=��ѧ������֮�ȣ�(2)��һ�������¿���Ϊ��־���ǣ��ٶ�����ɫ���ʲμӻ����ɵĿ��淴Ӧ��ϵ����ɫ���ٱ仯���ڶ�������̬���ʲμӻ����ɵĿ��淴Ӧ��ϵ������Ӧǰ�������ϵ������ȣ���������ƽ����Է�������M�ͷ�Ӧ��ѹP����(���º���)���۶��ں��¾�����ϵ����ϵ���¶Ȳ��ڱ仯��(3)������Ϊ�жϱ�־���ǣ��ٸ����ʵ����ʵ�����Ũ�ȱ仯��Ӧ����֮��=��ѧ������֮�� (�κ�����¾�����)��������̬���ʲμӻ����ɵķ�Ӧ������Ӧǰ�������ϵ������ȣ���������ƽ����Է�������M�ͷ�Ӧ��ѹP����(���º���)��
�����Ѷȣ�һ��
5��ѡ���� ����ͼʾ���Ӧ�������������
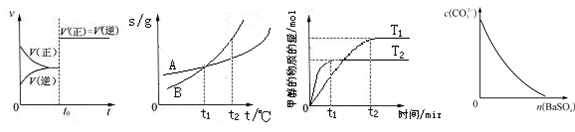
ͼ6?ͼ7?ͼ8?ͼ9
A��ͼ6��ʾ�Ѵ�ƽ���ij��Ӧ����t0ʱ�ı�ijһ������Ӧ������ʱ��仯����ı�����������Ǽ��������Ҳ�����Ǹı�ѹǿ
B��ͼ7��ʾA��B�����ʵ��ܽ�����¶ȱ仯�������t1��ʱA��B�ı�����Һ�ֱ�������t2��ʱ�����ʵ���������B>A
C��ͼ8��ʾ������������ͬʱ���ֱ���T1��T2�¶�����CO2��H2�ϳɼ״������ʵ�����ʱ��仯�������CO2��H2�ϳɼ״������ȷ�Ӧ
D��ͼ9��ʾ�ڱ���Na2CO3��Һ����BaSO4�������Һ��c(CO32-)��Ũ�ȱ仯
�ο��𰸣�A
���������B�û���µ����ʼ��룬���ܽ���б仯������������û�иı䣬�ʴ���C�T1��T2�ĸ����ĸ�С��֪�����жϣ��ʴ���D�BaSO4��BaCO3���ܣ�CO32-Ũ�Ȳ���䣬�ʴ�����ѡA��
���������⿼���Ϊ�ۺϣ���ͼ����γɿ��黯ѧƽ���ƶ������Լ�Ԫ�ػ�����֪ʶ����Ŀ�Ѷ��еȣ�ע����շ�Ӧ��ԭ����
�����Ѷȣ���