微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组离子,在溶液中能大量共存的是
A.Ba2+、K+、CO32-、Cl-
B.S2-、Cl-、Na+、H+
C.Na+、H+、I-、SO4-
D.Ca2+、Fe3+、NO3-、SCN-
参考答案:C
本题解析:分析:根据离子之间不能结合生成沉淀、气体、水、弱电解质,不能生成络离子等,则能大量共存,以此来解答.
解答:A.因Ba2+、CO32-结合生成沉淀,则不能大量共存,故A错误;
B.因S2-、H+结合生成弱电解质,则不能共存,故B错误;
C.因该组离子之间不反应,能共存,故C正确;
D.因Fe3+、SCN-结合生成络离子,则不能共存,故D错误;
故选C.
点评:本题考查离子的共存,熟悉复分解反应发生的条件是解答本题的关键,题目难度不大.
本题难度:简单
2、选择题 下列各组物质中化学键的类型相同的是
A.HCl、MgCl2
B.Na2O、CO2
C.CaCl2、H2O
D.NH3、H2O
参考答案:D
本题解析:A中氯化氢为共价键,氯化镁为离子键;B、氧化钠为离子键,二氧化碳为共价键;C、氯化钙为离子键,水中为共价键;D、氨气和水中都只有共价键。
点评:本题的解题思路需要学生判断化合物的类型,进而推出化学键的类型。有一些物质的化学键比较容易混淆,比如氯化氢中为共价键。一般来说共价化合物中只有共价键,而非金属元素与非金属元素一般组成共价化合物,除了铵盐等。金属元素与非金属大多组成离子 化合物。
本题难度:简单
3、填空题 (10分)在NaCl、NaOH、N2、H2S、Na2O2中,只含有离子键的是?,只含有极性键的是?,只含有非极性键的是?,既含有离子键又有极性键的是?,既含有离子键又有非极性键的是?。
参考答案:NaCl? H2S? N2? NaOH? Na2O2
本题解析:考查化学键的概念及判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键。所以在NaCl、NaOH、N2、H2S、Na2O2中含有的化学键分别为离子键、离子键和极性键、非极性键、极性键、离子键和非极性键。
本题难度:一般
4、判断题 (10分)用“√”或“×”判断下列说法是否正确。
(1)一个D2O分子所含的中子数为8。
(2)HI、HBr、HCl、HF的稳定性依次增强。
(3)同主族元素从上到下,单质的熔点逐渐降低。
(4)常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。
(5)从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。
(6)将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。
(7)在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。
(8)二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。
(9)用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。
(10)苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。
参考答案:(1)×(2)√(3)×(4)×(5)×(6)×(7)√(8)√(9)√(10)√
本题解析:一个D2O分子所含的中子数为1×2+8=10,(1)不正确;同主族自上而下非金属性逐渐增强,相应氢化物的稳定性逐渐增强,(2)正确;同主族元素从上到下,单质的熔点有的逐渐降低,例如碱金属,有的逐渐升高,例如卤素,(3)不正确;加热时钠和氧气反应,生成物的是过氧化钠,(4)不正确;断开化学键要吸热,形成化学键要放热,(5)不正确;原电池电子从负极经导线传递到正极,所以溶液中的阳离子向正极移动,(6)不正确;在可逆反应中,增大反应物的浓度,可以提高其它物质的转化率,(7)正确;如果甲烷是平面正方形结构,则二氯甲烷就有2种同分异构体,(8)正确;甲烷和乙烯中的含碳量不同,燃烧现象不同,乙烯含有碳碳双键,能使酸性高锰酸钾溶液褪色,(9)正确;只要含有碳碳双键,就能和溴水发生加成反应,也能使酸性高锰酸钾溶液褪色,(10)正确。
本题难度:简单
5、选择题 已知断裂1 mol H―H键吸收的能量为436 kJ,断裂1 mol H―N键吸收的能量为391 kJ,根据化学方程式:N2(g)+3H2(g)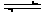 2NH3(g) ΔH=-92.4 kJ・mol-1,则断裂1 mol N≡N键吸收的能量是
2NH3(g) ΔH=-92.4 kJ・mol-1,则断裂1 mol N≡N键吸收的能量是
A.431 kJ
B.945.6 kJ
C.649 kJ
D.869 kJ