��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����H++OH-��H2O��ʾ����
A��Ba(OH)2��Һ��ϡH2SO4�ķ�Ӧ
B��NaOH��Һ�����ᷴӦ
C��Cu(OH)2��ϡH2SO4�ķ�Ӧ
D��NaOH��Һ��CO2�ķ�Ӧ
2��ѡ���� �������ӷ���ʽ��ȷ���� ��?��
A��NH4HCO3��Һ�����NaOH��Һ��Ӧ��NH 4++ OH�D��NH3��+ H2O
B���ö��Ե缫��ⱥ���Ȼ�����Һ��2Cl�D + 2H +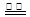 H2��+ Cl2��
H2��+ Cl2��
C����Fe��NO3��3��Һ�м��������HI��Һ��2Fe3++2I�D�� 2Fe2++I2
D��Na2SO3��Һʹ����KMnO4��Һ��ɫ��5SO32�D + 6H+ + 2MnO4�D��5SO42�D + 2Mn2+ +3H2O
3��ѡ���� �������ӷ���ʽ��ȷ����
[? ]
A��������̼��������Һ��Ӧ��2CH3COOH��CO32-==2CH3COO-��CO2����H2O
B��������Һ������������ͭ��Ӧ��2H+��Cu(OH)2==Cu2+��2H2O
C����������Һ��ͨ������������̼��2C6H5O-��CO2��H2O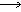 2C6H5OH��CO32-
2C6H5OH��CO32-
D����ȩ��Һ��������������Һ���ȣ�
HCHO+4[Ag(NH3)2]+��4OH-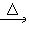 CO32-��2NH4+��4Ag����6NH3��2H2O
CO32-��2NH4+��4Ag����6NH3��2H2O
4��ѡ���� ���з�Ӧ�У����ӷ���ʽ��ȷ���ǣ�������
A������ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2��
B��̼��Ƹ����ᷴӦ��CaCO3+2H+�TCa2++2H2O+2CO2��
C��ϡ���������������Һ��Ӧ��H++OH-�TH2O
D������������Һ��ϡ���ᷴӦ��Ba2++SO42-�TSO4��
5������� ��ͭ��CuFeS2������ͭ���仯�������Ҫԭ��֮һ���������Ʊ������Ļ����
��1��ұ��ͭ�ķ�ӦΪ8CuFeS2��21O2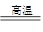 8Cu��4FeO��2Fe2O3��16SO2
8Cu��4FeO��2Fe2O3��16SO2
��CuFeS2��Fe�Ļ��ϼ�Ϊ+2����Ӧ�б���ԭ��Ԫ����?����Ԫ�ط��ţ���
��2������ұ�������в�������SO2�����д���������������?������ţ���
a���߿��ŷ�? b�������Ʊ�����
c���ô�����Һ������Na2SO3? d����Ũ��������?
��3����������أ�K2S2O8������ǿ�����ԣ��ɽ�I������ΪI2��S2O82����2I��=2SO42����I2
ͨ���ı䷴Ӧ;����Fe3���ɴ�������Ӧ���������ӷ���ʽ��ʾFe3����������Ӧ�Ĵ����̡�?��
?��
��������ƽ��ÿ��1�֣���
��4�����û�ͭ��ұ��ͭ������¯����Fe2O3��FeO��SiO2��Al2O3�����Ʊ�Fe2O3������Ϊ
����ϡ�����ȡ¯�������ˡ�
����Һ���������ټ������NaOH��Һ�����ˣ�������ϴ�ӡ�������յá�
��������Ϣ�ش��������⣺ѡ���ṩ���Լ������ʵ����֤¯���к���FeO��
�ṩ���Լ���ϡ����?ϡ����? KSCN��Һ? KMnO4��Һ? NaOH��Һ?��ˮ
��ѡ�Լ�Ϊ?��֤��¯���к��е�ʵ������Ϊ?
?��