微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一密闭容器中进行反应:2SO2(g)+O2(g)

2SO3(g)?测得开始时,SO2、O2、和SO3的浓度分别为0.2mol?L-1、0.1mol?L-1、0.2mol?L-1,在反应过程中不断测该容器中各物质的浓度,下列测定数据肯定不正确的是( )
A.O2为0.15mol?L-1
B.SO2为0.25mol?L-1
C.SO3为0.4mol?L-1
D.O2、SO3的浓度相等
参考答案:该题2SO2(g)+O2(g)?2SO3(g)是一个可逆反应.假设SO2(g)和O2(g)全部转化为SO3(g).?
? 2SO2(g)+O2(g)?2SO3(g)?
初始? 0.2mol?L-1 0.1mol?L-1 0.2mol?L-1
变化? 0.2mol?L-1 0.1mol?L-1 0.2mol?L-1
终了? 0? 0? 0.4mol?L-1
?
假设SO3(g)全部转化为SO2(g)和O2(g)
? 2SO2(g)+O2(g)?2SO3(g)?
初始? 0.2mol?L-1 0.1mol?L-1 0.2mol?L-1
变化? 0.2mol?L-1 0.1mol?L-1 0.2mol?L-1
终了? 0.4mol?L-1 0.2mol?L-1 ?0
该反应是一个可逆反应,无论向正反应方向进行还是向逆反应方向进行.实际不可能100%转化.
综上情况可知:0<n(SO2)<0.4mol?L-1 ;0<n(O2)<0.2mol?L-1 ;0<n(SO3)<0.4mol?L-1 .
A.O2为0.15mol?L-1 在范围内,不符合条件,故A不选;
B.SO2为0.25mol?L-1在范围内,不符合条件,故B不选;
C.SO3为0.4mol?L-1 不在范围内,故C测定数据肯定不正确,故C选;
D.O2、SO3的浓度相等,需平衡向逆反应方向进行:
? 2SO2(g)+O2(g)?2SO3(g)?
初始? 0.2mol?L-1 0.1mol?L-1 0.2mol?L-1
变化? 2X? X? 2X
终了? 0.2+2X?0.1+X? 0.2-2X
O2、SO3的浓度相等;0.1+X=0.2-2X?
? X=0.1/3 mol?L-1
?此时:
SO2:0.2+2X=0.2+0.2/3 ?mol?L-1;O2:0.1+X=0.1+0.1/3; SO3:0.2-0.1/3 mol?L-1
符合0<n(SO2)<0.4mol?L-1 ;0<n(O2)<0.2mol?L-1 ;0<n(SO3)<0.4mol?L-1 范围.
故D不选.
故选C.
本题解析:
本题难度:一般
2、选择题 下列关于化学反应的自发性叙述中正确的是
[? ]
A.焓变小于0而熵变大于0的反应肯定是自发的
B.焓变和熵变都小于0的反应肯定是自发的
C.焓变和熵变都大于0的反应肯定是自发的
D.熵变小于0而焓变大于0的反应肯定是自发的
参考答案:A
本题解析:
本题难度:简单
3、填空题 有A、B、C、D四个反应:
反应
| A
| B
| C
| D
|
ΔH/(kJ・mol-1)
| 10.5
| 1.80
| -126
| -11.7
|
ΔS/(J・mol-1・K-1)
| 30.0
| -113.0
| 84.0
| -105.0
|
?
则在任何温度下都能自发进行的反应是 ;任何温度下都不能自发进行的反应是 ;另两个反应中,在温度高于 ℃时可自发进行的反应是 ;在温度低于 ℃时可自发进行的反应是 。?
参考答案:C B 77 A -161.6 D
本题解析:放热的熵增反应在任何温度下都能自发进行,吸热的熵减反应在任何温度下都不能自发进行。放热的熵减反应在低温下能自发进行,吸热的熵增反应在高温下可以自发进行,具体温度可以根据ΔH-TΔS=0计算出来。
本题难度:一般
4、选择题 下列过程是非自发的是
[? ]
A.水由高处向低处流
B.天然气的燃烧
C.铁在潮湿空气中生锈
D.室温下水结成冰
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列说法正确的是
A.ΔH>0,ΔS>0的反应任何条件都是非自发反应;
B.因N2(g)+3H2(g)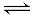 2NH3(g)△H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ
2NH3(g)△H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ
C.一定温度下,在固定体积密闭容器中,发生反应:2SO2(g)+O2(g)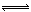 2SO3(g) △H<0,当v正(SO2)= v正(SO3)时,说明该反应已达到平衡状态
2SO3(g) △H<0,当v正(SO2)= v正(SO3)时,说明该反应已达到平衡状态
D.H2标准燃烧热△H="-285.8" kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)==2H2O(g) △H=-571.6 kJ・mol-1