��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����й�̼���ƻ�̼�������ܷ���ˮ��Ĺ۵���ȷ����
A����һ�������£�Na2CO3��Һ����ˮ��ƽ�⣺CO32-��H2O HCO3-��OH����ͨ��CO2��ƽ�⳯����Ӧ�����ƶ�
HCO3-��OH����ͨ��CO2��ƽ�⳯����Ӧ�����ƶ�
B��25��ʱ��Ũ�Ⱦ�Ϊ0.2 mol/L��NaHCO3��Na2CO3��Һ�У�ֻ���ڵ���ƽ�⣬������ˮ��ƽ��
C���ȵĴ���Һȥ����Ч���ã���Ϊ���ȿ�ʹCO32-��ˮ��̶�������Һ������ǿ��ȥ��������
D��pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��c(NaOH)��c(CH3COONa)��c(Na2CO3)
�ο��𰸣�A
���������A����һ�������£�Na2CO3��Һ����ˮ��ƽ�⣺CO32-��H2O HCO3-��OH����ͨ��CO2������OH��������OH��Ũ�ȣ�ƽ�⳯����Ӧ�����ƶ���A��ȷ��B��25��ʱ��Ũ�Ⱦ�Ϊ0.2 mol/L��NaHCO3��Na2CO3��Һ�У��ȴ���HCO3-��ˮ�ĵ���ƽ�⣬Ҳ����HCO3-��CO32-��ˮ��ƽ�⣬B����ȷ��C���ȵĴ���Һȥ����Ч���ã���Ϊ���ȿ�ʹCO32-��ˮ��̶�������Һ������ǿ��ȥ������ǿ��C����ȷ��D������������ǿ���̼���Ƶ�ˮ��̶ȴ��ڴ����Ƶ�ˮ��̶ȣ�����pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��c(NaOH)��c(Na2CO3)��c(CH3COONa)��D����ȷ����ѡA��
HCO3-��OH����ͨ��CO2������OH��������OH��Ũ�ȣ�ƽ�⳯����Ӧ�����ƶ���A��ȷ��B��25��ʱ��Ũ�Ⱦ�Ϊ0.2 mol/L��NaHCO3��Na2CO3��Һ�У��ȴ���HCO3-��ˮ�ĵ���ƽ�⣬Ҳ����HCO3-��CO32-��ˮ��ƽ�⣬B����ȷ��C���ȵĴ���Һȥ����Ч���ã���Ϊ���ȿ�ʹCO32-��ˮ��̶�������Һ������ǿ��ȥ������ǿ��C����ȷ��D������������ǿ���̼���Ƶ�ˮ��̶ȴ��ڴ����Ƶ�ˮ��̶ȣ�����pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��c(NaOH)��c(Na2CO3)��c(CH3COONa)��D����ȷ����ѡA��
�����Ѷȣ�һ��
2��ѡ���� ����0.1mol?L-1��NH4��2SO4��Һ������˵����ȷ�ģ�������
A����Һ�д��ڵ���ƽ㕣���NH4��2SO4?NH4++SO42-
B������Һ�еμ�����Ũ���ᣬc��NH4+����c��SO42-��������
C����ˮϡ�ͣ���Һ���������ӵ�Ũ�Ⱦ���С
D����Һ�У�c��SO42-��=2c��NH4+��+2c��NH3?H2O��
�ο��𰸣�A���������ǿ���������ȫ���룬�õȺ����ӣ�����NH4��2SO4�TNH4++SO42-����A����
B������Һ�еμ�����Ũ���ᣬ����������Ӻ���������ӣ����������Ӷ�笠����ӵ�ˮ��ƽ��NH4++H2O?NH3?H2O+H+�����������ã�����c��NH4+����c��SO42-��������B��ȷ��
C����ˮϡ�Ͷ�ˮ��ƽ��NH4++H2O?NH3?H2O+H+�ٽ����ã�����ϡ���̻ᵼ����Һ��������������Լ�������������������Ũ�Ȼ�����C����
D������Һ�е������غ㣺2c��SO42-��=c��NH4+��+c��NH3?H2O������D����
��ѡ��B��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ʹ0.1mol/L��NaHCO3��Һ��c(H+)��c(CO32-)��c(HCO3-)�����٣��䷽����
[? ]
A��ͨ�������̼����
B�������������ƹ���
C��ͨ���Ȼ�������
D�����뱥��ʯ��ˮ
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� �Ƚ�������Һ��pH? (�����������������=����
(1)25�桢1mol/LFeCl3��Һ_____80�桢1mol/LFeCl3��Һ��
(2)0��1mol/L(NH4)2CO3��Һ______0��1mol/L Na2CO3��Һ��
(3)0��1mol/LNH4Cl��Һ______0��01mo1/L NH4Cl��Һ��
(4)0��1mol/LNa2CO3��Һ______0��1mol/L NaHCO3��Һ��
A? >? <? <? >? B? > > > >? C? <? >? <? >? D <? <? >? >
�ο��𰸣�A
������������ȴٽ�ˮ�⣬���ԣ�1�����ߵ�����ǿ��NH4��ˮ�������ԣ�����(2)�к��ߵļ���ǿ���Ȼ�淋�Ũ��Խ��ˮ��̶�ԽС��������Խǿ����ˣ�3����ǰ�ߵ�����ǿ��̼���Ƶ�ˮ��̶ȴ���̼�����Ƶģ�����(4)��ǰ�ߵļ���ǿ����ѡA��
�����Ѷȣ�һ��
5��ѡ���� ������Һ���й��������ʵ���Ũ�Ȼ���������ϵ��ȷ����(�� ��)
A��NaHSO3��NaHCO3�����Ի����Һ��(S��C����R��ʾ):c(Na+)=c(HR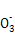 )+2c(R
)+2c(R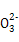 )
)
B�������½������ơ���������Һ��Ϻ�,��Һ������,���Ϻ���Һ��:c(Na+)��c(Cl-)��c(CH3COOH)
C�����������ʵ���Ũ����ȵĢ�(NH4)2CO3����(NH4)2SO4����(NH4)2Fe(SO4)2������Һ��c(N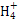 ):�٣��ۣ���
):�٣��ۣ���
D������������ʵ���Ũ�ȵ�NaClO��Һ��NaCl��Һ����������:Nǰ��N��
�ο��𰸣�A
���������ѡ��A�л��Һ�еĵ���غ�ʽΪc(H+)+c(Na+)=c(OH-)+c(HR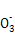 )+2c(R
)+2c(R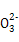 ),��������Һ��c(H+)=c(OH-),���ѡ��A��ȷ��ѡ��Bͬ��������д�������Һ�еĵ���غ�ʽ:c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(CH3COO-),��������Һ������,��c(H+)=c(OH-),��˻����Һ��Ӧ��c(Na+)=c(Cl-)+c(CH3COO-),���������غ�ɵ�c(Na+)=c(CH3COOH)+c(CH3COO-),������c(Na+)��c(Cl-)=c(CH3COOH),ѡ��B������ѡ��C,Fe2+�Ĵ��ڻ�����N
),��������Һ��c(H+)=c(OH-),���ѡ��A��ȷ��ѡ��Bͬ��������д�������Һ�еĵ���غ�ʽ:c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(CH3COO-),��������Һ������,��c(H+)=c(OH-),��˻����Һ��Ӧ��c(Na+)=c(Cl-)+c(CH3COO-),���������غ�ɵ�c(Na+)=c(CH3COOH)+c(CH3COO-),������c(Na+)��c(Cl-)=c(CH3COOH),ѡ��B������ѡ��C,Fe2+�Ĵ��ڻ�����N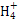 ��ˮ��,C
��ˮ��,C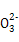 �Ĵ��ڻ�ٽ�N
�Ĵ��ڻ�ٽ�N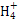 ��ˮ��,���ѡ��C�����ݵ���غ��֪ѡ��D�Ǵ���ġ�
��ˮ��,���ѡ��C�����ݵ���غ��֪ѡ��D�Ǵ���ġ�
�����Ѷȣ�һ��