|
|
|
高考化学知识点整理《盐类水解的原理》高频试题强化练习(2017年最新版)(五)
2017-09-25 19:14:58
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/ c(HCO3-)的比值保持增大
②浓度均为0.1 mol・L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO )+c(HCO )+c(HCO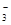 )] )]
③在0.1 mol・L-1氨水中滴加0.lmol・L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol・L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
A.①④
B.②⑤
C.①③
D.②④
|
2、选择题 将AlCl3溶液和NaAlO2溶液分别蒸干并灼烧,所得产物主要成分为
A.都是Al(OH)3
B.前者是Al2O3,后者是NaAlO2
C.都是Al2O3
D.前者是AlCl3,后者是NaAlO2
3、选择题 下列各组溶液中,微粒的物质的量浓度关系正确的是
A.0.1mol/L Na2CO3溶液:c(OH―) = c(HCO3―) + c(H+)+ c(H2CO3)
B.0.1mol/L NH4Cl溶液:c(NH4+)= c(Cl―)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO―)>c(H+)>c(OH―)
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)= c(NO3―)
|
4、实验题 (1)(2分)甲同学在用FeSO4固体配制FeSO4溶液时,除了加入蒸馏水外,还需加 和 试剂(填化学式)
(2)(2分)乙同学为标定某醋酸溶液的准确浓度,用0.2000 mol・L―1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号
| 1
| 2
| 3
| 4
|
消耗NaOH溶液的体积(mL)
| 20.05
| 20.00
| 18.80
| 19.95
|
则该醋酸溶液的准确浓度为
。(保留小数点后四位)
(3)丙同学利用:5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O反应,用KMnO4溶液滴定某样品进行铁元素含量的测定。
①(2分)设计的下列滴定方式,最合理的是_____。(夹持部分略去)(填字母序号)
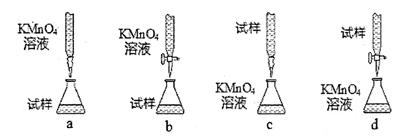
②(2分)判断滴定终点的依据是
。
5、填空题 (12分)(1)物质的量浓度相同的三种盐NX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是 。
(2)比较下列溶液的pH(填“>”“<”或“=”):
①0.1 mol・L-1Na2CO3溶液 0.1 mol・L-1NaHCO3溶液
②0.1 mol・L-1NH4Cl溶液 0.01 mol・L-1NH4C1溶液
(3)把a、b、c、d四块金属片浸泡在稀H2SO4中,用导线两两相连,可以组成各种原电池。若a、b相连,a为负极;c、d相连,c极发生氧化反应;a、c相连,c为正极;b、c相连,电流由c极流向b极,则这四种金属的活动性由强到弱的顺序为 。
(4)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成份是 。
(5)氯化铁溶液呈 性(填“酸”、“碱”或“中”),原因是(用离子方程式表示):
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,溶液的pH 7(填“>”“<”或“=”),离子反应总方程式为: 。
