1、填空题 如图为高温超导领域里的一种化合物――钙钛矿晶体结构,该结构是具有代表性的最小重复单位。
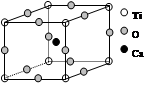
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有?、?个。
(2)该晶体结构中,元素氧、钛、钙的离子个数比是?。该物质的化学式可表示为?。
(3)若钙、钛、氧三元素的相对原子质量分别为a,b,c,晶体结构图中正方体边长(钛原子之间的距离)为dnm(1nm=10-9m),则该晶体的密度为?g/cm3(阿伏加德罗常数用NA表示)。
参考答案:7分 除注明外每空1分)(1) 6;8?(2) 3:1:1;CaTiO3? (3) (3分)
(3分)
本题解析:(1)由于1个顶点可以形成8个立方体,所以根据晶胞结构可知,在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有6个和8个。
(2)根据晶胞结构并依据均摊法可知,该晶体结构中,元素氧、钛、钙的离子个数分别是12× =3个、8×
=3个、8× =1个、1个,即晶体结构中,元素氧、钛、钙的离子个数比是3:1:1,所以该物质的化学式可表示为CaTiO3。
=1个、1个,即晶体结构中,元素氧、钛、钙的离子个数比是3:1:1,所以该物质的化学式可表示为CaTiO3。
(3)根据以上分析可知, ,解得密度ρ=
,解得密度ρ= g/cm3。
g/cm3。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。
本题难度:一般
2、选择题 已知CsCl晶体的密度为ρg/cm3,NA为阿伏加德罗常数的值,相邻的两个Cs+的核间距为acm(如右图所示),则CsCl的相对分子质量可表示为
A.
B.
C.
D.NA・a3・ρ
参考答案:D
本题解析:根据氯化铯的晶胞可知,该晶胞中含有8个氯离子和铯离子,所以有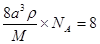
,解得M=NA・a3・ρ,所以答案选D。
本题难度:一般
3、选择题 下列各组中的两种固态物质熔化或升华时,克服的微粒间相互作用力属于同种类型的是
A.碘和氯化钾
B.金刚石和重晶石
C.二氧化硅和干冰
D.软脂酸甘油酯和冰醋酸
参考答案:D
本题解析:A错,碘为破坏分子间作用力,而氯化钾为破坏离子键;B错,金刚石为破坏共价键,重晶石为破坏离子键;C错,二氧化硅为破坏共价键,干冰为破坏分子间作用力;D正确,均为破坏分子间作用力;
本题难度:一般
4、填空题 第三主族元素包括B、Al、Ga、In、Tl。
(1)在硼酸B(OH)3分子中,B原子与3个羟基相连,其晶体为层状结构。则分子中B原子杂化轨道的类型为?,同层分子间的主要作用为?。
(2)氯化铝在气态中常以二聚分子Al2Cl6形式存在,在Al2Cl6分子中存在的化学键的类型有 ?、?。
(3)砷化镓属于第三代半导体,它能直接将电能转化为光能,其晶胞结构如右图所示。
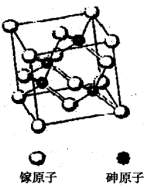
①Ga的基态原子的核外电子排布式为?。
②在砷化镓的晶胞结构中,镓原子的配位数为____?。
③在砷化镓的晶胞结构中,与同一砷原子相连的镓原子构成的空间构型为?。
参考答案:(1)SP2?氢键?(2)极性共价键、配位键
(3)①1S22S22P63P63d104s24p1?②4?③正四面体
本题解析:略
本题难度:一般
5、选择题 BeCl2熔点较低,易升华,溶于醇和醚,其化学性质与AlCl3相似。由此可推测BeCl2
A.熔融态不导电
B.水溶液呈中性
C.熔点比BeBr2高
D.不与氢氧化钠溶液反应
参考答案:A
本题解析:A、BeCl2熔点较低,易升华,溶于醇和醚,说明该化合物形成的晶体是分子晶体,熔融态不导电,A正确;B、该化合物的化学性质与AlCl3相似,而氯化铝溶液显酸性,因此其水溶液也呈酸性,B不正确;C、BeCl2与BeBr2形成的晶体均是分子晶体,后者的相对分子质量大,熔点高于BeCl2,C不正确;D、氯化铝能与氢氧化钠溶液反应生成偏铝酸钠和水,则该化合物也与氢氧化钠溶液反应,D不正确,答案选A。
本题难度:简单