|
高考化学知识点归纳《未知》高频试题巩固(2017年最新版)(四)
2017-11-05 20:34:18
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 有时候,将氧化还原方程式拆开写成两个“半反应”。下面是一个“半反应”式:
(? ) +(? )H++(? )e-="===(?" )NO+(? )H2O,该式的配平系数是(?) +(? )H++(? )e-="===(?" )NO+(? )H2O,该式的配平系数是(?)
A.1,3,4,2,1
B.2,4,3,2,1
C.1,6,5,1,3
D.1,4,3,1,2
参考答案:D
本题解析:本题灵活考查了氧化还原反应中的守恒观。氧化还原反应中遵循质量守恒,得失电子守恒。半反应也不例外。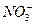 中的N元素由+5价降至+2价,需得到3个电子,再由O元素守恒可确定答案为D。做好此题可为以后书写电化学中的半极反应打好基础。 中的N元素由+5价降至+2价,需得到3个电子,再由O元素守恒可确定答案为D。做好此题可为以后书写电化学中的半极反应打好基础。
本题难度:一般
2、填空题 Ⅰ.2011年4月27日某市工商局查获400克袋装中老年补钙营养奶粉1 401包。这种奶粉被鉴定为所含亚硝酸盐残留量高出正常值7.8倍,长期食用可能致癌。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是_____,若有0.75 mol的还原剂被氧化,则被还原的氧化剂有_____mol。
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①自来水;②淀粉碘化钾试纸;③淀粉;④白糖;⑤食醋;⑥白酒。进行实验时,必须选用的物质有____________。
(3)某工厂废切削液中含有2%~5%的NaNO2,直接排放会造成污染,下列试剂中_____(填序号)能使NaNO2转化为不引起二次污染的N2反应的化学方程式为________________________ (并标出电子转移的数目和方向)。
①NaCl ②NH4Cl ③H2O2 ④浓H2SO4
(4)下列离子在溶液中一定能大量共存的是________。
A.NH Cl- OH- CO Cl- OH- CO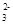
B.Fe2+ NO3- Cl- H+
C.CH3COO- NH H+ Cl- H+ Cl-
D.CH3COO- Na+ Cl- SO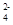
| Ⅱ.实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应式为
4CuI+Hg===Cu2HgI4+2Cu。
(1)上述反应产物Cu2HgI4中,Cu元素是________价。
(2) CuI可由Cu2+与I-直接反应制得,请配平下列反应的离子方程式:
 Cu2++ Cu2++ I-=== I-=== CuI+ CuI+ I I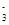
参考答案:Ⅰ(1)NaNO2 0.75 (2)②⑤
(3)② (4)D (4)D
Ⅱ.(1)+1 (2) 2Cu2++5I-===2CuI+I3-
本题解析:Ⅰ(1)根据反应的方程式可知,亚硝酸钠中氮元素的化合价从+3价降低到+2价,得到1个电子,所以亚硝酸钠是还原剂。HI中I元素的化合价从-1价升高到0价,失去1个电子,则根据电子得失守恒可知,若有0.75 mol的还原剂被氧化,则被还原的氧化剂有0.75mol。
(2)根据反应的方程式可知,该反应是在酸性条件下进行的,所以必须选用的物质有淀粉碘化钾试纸和食醋,答案选②⑤。
(3)使NaNO2转化为不引起二次污染的N2,这说明在反应中亚硝酸钠是氧化剂,得到电子,所以选择的应该是还原剂,NH4+中的氮元素处于最低价态,具有还原性,所以选择的试剂是氯化铵,即答案选②,反应的方程式是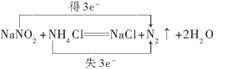 。 。
(4)A中的OH-与NH4+不能大量共存;B中溶液显酸性,则NO3-能氧化Fe2+不能大量共存;C中的CH3COO-和H+不能大量共存,所以答案选D。
Ⅱ.(1)在Cu2HgI4中,Hg显+2价,I是-1价,所以铜是+1价。
(2)在反应中铜的化合价从+2价降低到+1价,得到1个电子,而碘元素碘化合价从-1价升高到0价,失去1个电子,则根据电子的得失守恒可知,配平后的方程式应该是2Cu2++5I-===2CuI+I3-。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是准确标出有关元素的化合价变化情况,然后依据有关的概念,并结合电子得失守恒进行列式计算和判断即可。
本题难度:一般
3、选择题 向100 mL FeBr2溶液中通入标准状况下的 Cl2 3.36 L ,Cl2全部被还原,测得溶液中?c(Br-) =c(Cl-) ,则原 FeBr2溶液的物质的量浓度是(?)
A.0.75 mol/L
B.1.5 mol/L
C.2 mol/L
D.3 mol/L
参考答案:C
本题解析:设原 FeBr2溶液的物质的量浓度是x。由于亚铁离子的还原性强于溴离子的,因此氯水首先氧化的是亚铁离子,所以0.1x+(0.2x-0.3)=0.15×2,解得x=2mol/L,答案选C。
本题难度:一般
4、填空题 (15分)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
⑴SO2和O2反应制取SO3的反应原理为:2SO2+O2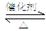 2SO3,在一密闭容器中一定时间内达到平衡. 2SO3,在一密闭容器中一定时间内达到平衡.
①该反应的平衡常数表达式为: .
②该反应达到平衡状态的标志是 .
A.v(SO2)=v(SO3) B.混合物的平均相对分子质 量不变
C.混合气体质量不变 D.各组分的体积分数不变
⑵某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触.

①B电极的电极反应式为 ;
②溶液中H+的移动方向由 极到 极;(用A、B表示)
⑶测定绿矾产品中含量的实验步骤:
a.称取5.7 g产品,溶解,配成250 mL溶液
b.量取25 mL待测液于锥形瓶中
c.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积40 mL
根据上述步骤回答下列问题:
①滴定时发生反应的离子方程式为(完成并配平离子反应方程式).
Fe2++ 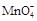 + ―― Fe3++ Mn2++ + ―― Fe3++ Mn2++
②用硫酸酸化的KMnO4滴定终点的标志是 .
③计算上述产品中FeSO4・7H2O的质量分数为 .
参考答案:⑴① ②BD ②BD
⑵①SO2+2H2O-2e-==SO42-+4H+ ②B A
⑶①5Fe2++1 +8H+===5Fe3++1Mn2++4H2O +8H+===5Fe3++1Mn2++4H2O
②滴定最后一滴酸性KMnO4时溶液呈淡紫色,半分钟内不褪色。 ③0.975或97.5%
本题解析:(1)①根据平衡常数的概念可知 。 。
②A项没有正逆反应速率,不能判断;B项混合物的平均相对分子质量反应前后不同,可以判断;C项混合气体的质量反应前后不变,不能判断;D项各组分的体积分数反应前后不同,可以判断。答案选BD。
(2)①根据B极的产物可以看出B极发生氧化反应,是负极,电极方程式为SO2+2H2O-2e-=SO42-+4H+。
②阳离子向正极移动,所以H+从B极向A极移动。
(3)①根据化合价升降法,方程式配平为5Fe2++1 +8H+===5Fe3++1Mn2++4H2O。 +8H+===5Fe3++1Mn2++4H2O。
②KMnO4本身有颜色,所以不需要指示剂,用本身的颜色就可以判断终点,当滴定最后一滴酸性KMnO4时溶液呈淡紫色,半分钟内不褪色时达到滴定终点。
③产品中FeSO4・7H2O的质量分数为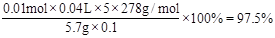 。 。
考点:化学平衡、原电池和氧化还原滴定
点评:本题综合性强,难度较大,非常锻炼学生的思维能力。
本题难度:困难
5、填空题 亚硝酸钠(NaNO2)又称工业盐,其外观类似食盐,但有剧毒.近年来,建筑工地多次发生民工误食工业盐而中毒的事件.利用如下反应可鉴别NaNO2和NaCl.
______KMnO4+______NaNO2+______H2SO4=______MnSO4+______K2SO4+______NaNO3+______H2O
(1)配平上述反应的化学方程式;
(2)指出该反应的氧化剂______;
(3)当有2mol氧化剂被还原时,则转移的电子是______mol.
参考答案:(1)该反应中,1mol高锰酸钾参加氧化还原反应得到4mol电子,1mol亚硝酸钠参加氧化还原反应失去2mol电子,所以得失电子的最小公倍数是10,则高锰酸钾的计量数是2,亚硝酸钠的计量数是5,其它原子根据原子守恒配平即可,所以该反应方程式为:2KMnO4+5NaNO2+3H2SO4=2MnSO4+1K2SO4+5NaNO3+3H2O.
故答案为:2;5;3;2;2;1;5;3.
(2)该反应中高锰酸钾得电子化合价降低,所以高锰酸钾是氧化剂.
故答案为:KMnO4.
(3)当有1mol高锰酸钾参加氧化还原反应时,转移5mol电子,所以当有2mol氧化剂被还原时,则转移的电子是10mol. 故答案为:10.
本题解析:
本题难度:简单
|  Cu2++
Cu2++ I-===
I-=== CuI+
CuI+ I
I