1、填空题 ⑴在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中,?是氧化剂; ?元素被氧化;? ________是氧化产物;7mol HCl参与反应时转移的电子总数为_____mol.
⑵反应11P +15CuSO4 +24H2O = 5Cu3P + 6H3PO4 +15H2SO4中32g CuSO4能氧化磷的质量为_________g.
参考答案:⑴K2Cr2O7; Cl;Cl2;3。(每空1分)
⑵1.24g.(2分)
本题解析:略
本题难度:简单
2、填空题 交警常用“司机饮酒检测仪”检查司机是否酒后驾车,其原理是硫酸酸化的重铬酸盐(Cr2O72-橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬。请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是 。
(2)写出碳和重铬酸钠高温反应的化学方程式 。
Cr2O3经铝热法还原制得金属铬的化学方程式是 。
(3)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是 。
(4)某Na2Cr2O7样品2.00g恰好和4.56gFeSO4完全反应,该样品的纯度为 。
参考答案:⑴2K2Cr2O7 + 3CH3CH2OH + 8H2SO4 = 2Cr2(SO4)3 + 3CH3COOH + 2K2SO4 + 11H2O。(3分)
⑵Na2Cr2O7 + 2C Cr2O3 + Na2CO3 + CO ↑;(3分)
Cr2O3 + Na2CO3 + CO ↑;(3分)
Cr2O3 + 2Al  2Cr + Al2O3(3分)
2Cr + Al2O3(3分)
⑶Cr2O72- + 6Fe2+ + 14H+ ==2Cr3+ + 6Fe3+ + 7H2O。(3分)
⑷65.5%
本题解析:略
本题难度:简单
3、选择题 2.8 g Fe全部溶于一定浓度、200 mL的HNO3溶液中,得到标准状况下的气体1.12 L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列有关判断正确的是( )。
A.反应后溶液中c(NO3-)=0.85 mol・L-1
B.反应后的溶液最多还能溶解1.82 g Fe
C.反应前HNO3溶液的浓度为1.0 mol・L-1
D.1.12 L气体是NO、NO2的混合气体
参考答案:AB
本题解析:据题意,硝酸过量:0.2 L×0.1 mol・L-1=0.02 mol,反应生成Fe3+:2.8 g÷56 g・mol-1=0.05 mol,A项中据反应后溶液中的电荷守恒,得c(NO3-)=(0.05 mol×3+0.02 mol×1)÷0.2 L=0.85 mol・L-1,该项正确;B项中反应后的溶液还能与铁发生反应的离子方程式为:
3Fe + 8H+ + 2NO3-=3Fe2++2NO↑+4H2O
3 ?8 2
0.02 mol×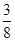 0.02 mol ? 0.17 mol(过量)
0.02 mol ? 0.17 mol(过量)
2Fe3+ + Fe = 3Fe2+
0.05 mol 0.025 mol
则最多能溶解铁:(0.02 mol×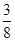 +0.025 mol)×56 g・mol-1=1.82 g,故该项正确;C项中据氮原子守恒,反应前HNO3溶液的浓度为(0.17 mol+1.12 L÷22.4 L・mol-1)÷0.2 L=1.1 mol・L-1,故该项错误;D项中反应前硝酸的溶液为稀溶液(c(HNO3)=1.1 mol・L-1),1.12 L气体应是NO气体,故该项错误。
+0.025 mol)×56 g・mol-1=1.82 g,故该项正确;C项中据氮原子守恒,反应前HNO3溶液的浓度为(0.17 mol+1.12 L÷22.4 L・mol-1)÷0.2 L=1.1 mol・L-1,故该项错误;D项中反应前硝酸的溶液为稀溶液(c(HNO3)=1.1 mol・L-1),1.12 L气体应是NO气体,故该项错误。
本题难度:一般
4、选择题 将铜银合金投入到稀HNO3溶液中,发生如下反应:
aCu+bAg+cNO3-+dH+=eCu2++fAg++gNO↑+hN2O↑+mH2O,下列关系式错误的是(? )
A.d-c="2a+f"
B.2e+b="3g+8h"
C.反应中消耗的硝酸的物质的量为(2e+f+g+h)mol
D.d="4g+10h"
参考答案:C
本题解析:略
本题难度:简单
5、选择题 三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体,无色、无臭,在潮湿空气中泄露会产生白雾、红棕色气体等现象,反应方程式为:aNF3+bNF3=c?+dHNO3+eHF。下列说法正确的是
A.反应方程式横线处物质为NO,且a=3、b=5、c=2、d=1、e=9
B.反应中被氧化与被还原的原子物质的量之比为2:1
C.若反应中生成0.2molHNO3,则反应共转移0.2mole-
D.反应中NF3是氧化剂,H2O是还原剂
参考答案:A
本题解析:红棕色气体为NO2;根据氮元素化合价升降情况,反应不可能直接产生NO2,故反应方程式空格处物质为NO,配平反应方程式为3NF3+5NF3=2NO+HNO3+9HF
本题难度:一般