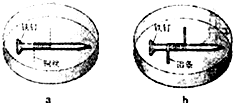
1������� ��3�֣��õ��߽�пƬ��ͭƬ���Ӻ����ϡ������Һ�У�������ԭ��أ��˵�صĸ�����?�������ĵ缫��Ӧʽ��?��
�ο��𰸣���
�����������
�����Ѷȣ���
2��ѡ���� ��ͼ��һ��أ������й�˵����ȷ���ǣ�������
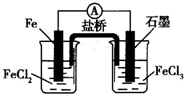
A���õ�ظ�����ӦΪ��2Fe2+-2e-�T2Fe3+
B������6.02��1023����ת��ʱ��Fe�缫����56g
C��ʯī�缫�Ϸ���������Ӧ
D��������K+����FeCl3��Һ
�ο��𰸣���ԭ����У�����������ʯī��������
A����������ʧ���ӷ���������Ӧ���缫��ӦʽΪ��Fe-2e-�TFe2+����A����
B������6.02��1023����ת��ʱ��Fe�缫���ٵ�����=6.02��10236.02��1023/mol��12��56g/mol=28g����B����
C��ʯī�������������������ӵõ��ӷ�����ԭ��Ӧ����C����
D��������K+���������������Һ��������FeCl3��Һ����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3������� ��5�֣���ͭƬ��пƬ������С�ձ������ߡ������ţ���������KCl������Һ���������ơ�ZnSO4��Һ��CuSO4��Һ���Ի���ԭ��ص�װ��ͼ����˵���乤��ԭ����
��ԭ���װ��ͼ�� �ƹ���ԭ����
�ο��𰸣���ԭ��ص�װ��ͼ��3�֣�

�ƹ���ԭ����2�֣���
����пʧ���ӣ�������������Ӧ��ʹ������������Zn2+��������ó��д��ݴ���������ɵ�Cl���������ص��ߴ��ݵ����������������磬����������CU2+��CU2+�ڸõ缫�õ��ӷ�����ԭ��Ӧ��ʹ�����������˸�����SO42����������ó��д��ݴ���������ɵ�K+��
�����������
�����Ѷȣ�һ��
4��ѡ���� ���и���װ���������ԭ��ص���
[? ]
A��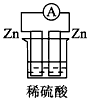
B��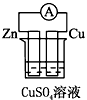
C��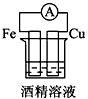
D��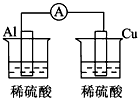
�ο��𰸣�D
���������
�����Ѷȣ���
5��ѡ���� ����ͼ��ʾ�����������Ʋ�ͬ���������������������У��ټ��뺬��������̪��NaCl����֬����Һ����ȴ���γ������������������ڿ����ƶ���������������ȷ���ǣ�������
A��a�������������ֺ�ɫ
B��b�������Ϸ�����ԭ��Ӧ
C��a��ͭ˿�Ϸ���������Ӧ
D��b���������������ݲ���