|
高中化学知识点大全《常见的化学电源》高频试题巩固(2017年最新版)(六)
2017-11-05 20:43:32
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 甲醇(CH3OH)燃料电池被认为是很有应用前景的燃料电池.下图是自呼吸式甲醇燃料电池工作示意图.电池总反应:2CH3OH+3O2=2CO2+4H2O,则图中进入c口的物质是( )
A.CH3OH
B.CO2
C.空气
D.H2O
| 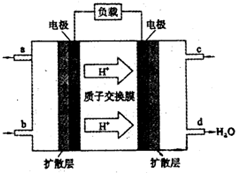
参考答案:燃料电池中,负极上是燃料失电子发生氧化反应,正极上是氧化剂得电子发生还原反应,
通过图片知,氢离子从左向右移动,说明b处通入的是甲醇,甲醇反应生成氢离子,氢离子到达d处和氧气反应生成水,所以c处通入的物质是氧气,氧气得电子发生还原反应,
故选C.
本题解析:
本题难度:一般
2、选择题 NA表示阿伏加德罗常数的值,下列说法正确的是
A.在0℃,101kPa的条件下,22.4LH2含有的分子数为NA
B.在同温同压下,22.4L的二氧化碳和32g氧气所含分子数都为NA
C.标准状况下,22.4L H2O的分子数为1NA
D.常温常压下,5.6 L CH4含有的分子数为0.25NA
参考答案:A
本题解析:
正确答案:A
A.正确,在0℃,101kPa的条件下(即标准状况),22.4LH2(1mol)含有的分子数为NA
B.不正确,在同温同压下,22.4L的二氧化碳,无法确是不是标准状况;
C.不正确,标准状况下, H2O为液体;
D. 不正确,应是标准状况,5.6 L CH4含有的分子数为0.25NA
本题难度:简单
3、填空题 (14分)已知CO2、SO2、NOx是对环境影响较大的气体,请你运用所学知识参与环境治理,使我们周围的空气更好。
(1)硫酸生产中,SO2催化氧化生成SO3,反应混合体系
中SO3的百分含量和温度的关系如右图所示(曲线上
点均为平衡状态)。由图可知:

①2SO2(g) + O2(g) 2SO3(g)的△H____0(填“>”或“<”),若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或“不移动”); 2SO3(g)的△H____0(填“>”或“<”),若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或“不移动”);
②若温度为T1时,反应进行到状态D时,v(正)_______v(逆)(填“>”、“<”或“=”);
③硫酸厂的SO2尾气用过量的氨水吸收,对SO2可进行回收及重新利用,反应的化学方程式为 、 ;
④新型氨法烟气脱硫技术是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。其优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为:________(只要求写一种);
(2)汽车尾气(含有烃类、CO、NOx等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。其前半部反应方程式为:
2CO+2NO  2CO2+N2。它的优点是 ; 2CO2+N2。它的优点是 ;
(3)有人设想用图所示装置,运用电化学原理将CO2、SO2转
化为重要化工原料。

①若A为CO2,B为H2,C为CH3OH,则正极电极反应式为
;
②若A为SO2,B为O2,C为H2SO4。科研人员希望每分钟
从C处获得100 mL 10 mol/L H2SO4,则A处通入烟气(SO2
的体积分数为1%)的速率为 L/min(标准状况)。
参考答案:(14分)
(1)① < ;(1分) 向左;(1分) ② > ;(2分)
③ SO2+H2O+2NH3 =(NH4)2SO3 、
(NH4)2SO3+H2SO4 =(NH4)2SO4+SO2↑+H2O ;(2分)
④(NH4)3PO4(或(NH4)2HPO4 、NH4H2PO4);(2分)
(2)使CO与NO反应,生成可参与大气生态环境循环的无毒气体;(2分)
(3) ① CO2+6H++6e-= CH3OH+H2O ;(2分) ② 2240 。(2分)
本题解析:(1)①根据图可判断随温度升高,三氧化硫的百分含量减小,说明升温平衡逆向移动,所以正向是放热反应,△H<0;在恒温、恒压条件下向上述平衡体系中通入氦气,使容器体积增大,各物质浓度均减小,相当于体系减小压强,平衡向左移动;
②若温度为T1时,反应进行到状态D时,三氧化硫的转化率未达平衡状态的转化率,所以反应正向进行,v(正)>v(逆);
③SO2尾气用过量的氨水吸收,先生成亚硫酸铵,再与硫酸反应又生成二氧化硫,化学方程式为SO2+H2O+2NH3 =(NH4)2SO3 、(NH4)2SO3+H2SO4 =(NH4)2SO4+SO2↑+H2O ;
(2)它的优点是使有毒气体转化为无毒气体;
(3)①若A为CO2,B为H2,C为CH3OH,则正极发生还原反应,元素化合价降低,所以是CO2发生还原反应生成甲醇,电极反应式为CO2+6H++6e-= CH3OH+H2O;
②A为SO2,则SO2+2H2O-2e-=H2SO4+2H+,每分钟从C处获得1mol H2SO4,则需要二氧化硫是22.4L(标准状况),SO2的体积分数为1%,所以A处通入烟气的速率是22.4L/min÷1%=2240L/min。
考点:考查化学平衡理论的应用,二氧化硫的吸收,电化学原理的应用及计算
本题难度:困难
4、填空题 (18分,每空3分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42― 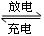 2PbSO4+2H2O 2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是______?______;电解液中H2SO4的浓度将变__?__;当外电路通过1 mol电子时,理论上负极板的质量增加___?___g。
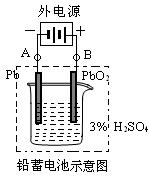
(2)电池使用一段时间后,若按图连接,则在A电极上生成___?__、B电极上生成__?__,此时铅蓄电池的正负极的极性将_?___。(填“不变”或“对掉”)
参考答案:(1)PbO2 +2e-+ 4H+ +SO42-="=" PbSO4 + 2H2O ;小;48?(2)Pb; PbO2 ;不变
本题解析:略
本题难度:一般
5、选择题 实验中需0.5 mol/L的NaOH溶液240 ml,配制时应选用容量瓶的规格和称取NaOH的质量分别是? ( )
A.240 ml ,4.8 g
B.250 ml ,5.0 g
C.500 ml ,10.0 g
D.任意规格,4.8 g
参考答案:B
本题解析:容量瓶有一定的规格,一般有100ml、250ml、500ml、1000ml等,所以,配制溶液240 ml时选用的容量瓶为250 ml ,进而可求得质量为5.0 g
本题难度:简单
| 